化合物 X 由 4 种元素组成。某兴趣小组按如图流程进行实验:
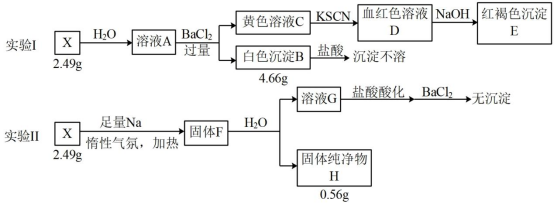
请回答:
(1) 组成 X 的元素有 , X 的化学式为 。
(2) 溶液 C 中溶质的成分是 ( 用化学式表示 ) ;根据 C→D→E 的现象,给出相应微粒与 阳离子结合 由弱到强的排序 。
(3)X 与足量 Na 反应生成固体 F 的化学方程式是 。
(4) 设计实验确定溶液 G 中阴离子 。
答案
(1) Fe 、 S 、 O 、 H FeH(SO 4 ) 2
(2) FeCl 3 、 HCl 、 BaCl 2 Cl - 、 H 2 O 、 SCN - 、 OH -
(3)2FeH(SO 4 ) 2 +40Na 2Fe+4Na 2 S+16Na 2 O+H 2
(4) 用玻璃棒蘸取溶液 G ,点在红色石蕊试纸上,若变蓝,说明存在 OH - ;取少量溶液 G ,加入足量 H 2 O 2 ,用盐酸酸化,再加入 BaCl 2 溶液,有白色沉淀,说明有 S 2-
【分析】 X 形成水溶液,与氯化钡反应生产白色沉淀,且沉淀不与盐酸反应说明生产硫酸钡,说明 X 含有硫酸根,溶液加入 KSCN 变红说明含有 Fe 3+ , B 为 4.66g 则为 0.02mol 硫酸钡,说明 X 含有 0.02mol 的硫酸根, H 中为 Fe 单质,即为 0.01mol , X 中含有 0.01molFe ,由此可知 X 中应含有 0.01 的 H ,据此分析解题。
【详解】( 1 )由分析可知,组成 X 的元素有: Fe 、 S 、 O 、 H ; X 的化学式为 FeH(SO 4 ) 2 ;
( 2 ) X 为 FeH(SO 4 ) 2 与氯化钡反应,溶液 C 中溶质的成分是 FeCl 3 、 HCl 以及过量的 BaCl 2 ;根据 C 为溶液,铁离子在水中会水解, C→D 形成络合物, D→E 形成沉淀,相应微粒与阳离子结合由弱到强的排序: Cl - 、 H 2 O 、 SCN - 、 OH - ;
( 3 ) X 与足量 Na 反应生成固体 F 的化学方程式是: 2FeH(SO 4 ) 2 +40Na 2Fe+4Na 2 S+16Na 2 O+H 2 ;
( 4 )设计实验确定溶液 G 中阴离子:用玻璃棒蘸取溶液 G ,点在红色石蕊试纸上,若变蓝,说明存在 OH - ;取少量溶液 G ,加入足量 H 2 O 2 ,用盐酸酸化,再加入 BaCl 2 溶液,有白色沉淀,说明有 S 2- 。