依据氧化还原反应: 2Ag + + Cu=Cu 2 + + 2Ag 设计的原电池如图所示。请回答下列问题:
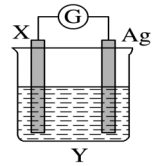
(1) 电解质溶液 Y 是 _______ 。
(2) 银电极为电池的 _______ 极,发生的电极反应式为 _______ ;
(3) 外电路中的电子 _______( 填 “ 流出 ” 或 “ 流入 ”)Ag 电极。
(4) 当有 1.6g 铜溶解时,银棒增重 _______g 。
答案
(1) 硝酸银
(2) 正 Ag + + e - =Ag
(3) 流入
(4)5.4g
【分析】由总反应可知反应中铜做负极,银离子在银电极上得到电子变为银单质。
( 1 )
由反应可知电解质溶液 Y 应为硝酸银溶液;
( 2 )
由总反应可知,银电极为电池的正极;
电极反应为: Ag + + e - =Ag ;
( 3 )
电子由负极流出,流入倒正极, Ag 为正极,所以外电路中的电子应流入 Ag 电极;
( 4 )
1.6gCu 的物质的量为 0.025mol ,每个 Cu 原子转移两个电子,转移的电子数为 0.05mol ,每个 Ag 原子得到 1 个电子生成 Ag 单质,则生成的 Ag 单质物质的量为 0.05mol ,质量为 5.4g ,所以增重的质量为 5.4g 。