将 0.1mol 镁和铝的混合物溶于 100mL2mol·L -1 硫酸中,然后滴加 1mol·L -1 NaOH 溶液。回答下列问题:
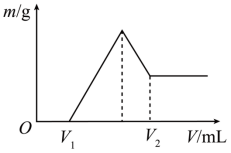
(1) 若在滴加 NaOH 溶液的过程中,沉淀质量随加入 NaOH 溶液体积的变化如图所示。
① 有关反应的离子方程式为 ____ 。
② 当 V 1 =160 时,金属粉末中 n(Mg)=____mol , V 2 =___ 。
(2) 若在滴加 NaOH 溶液的过程中,欲使 Mg 2+ 、 Al 3+ 刚好沉淀完全,则滴入 NaOH 溶液的体积为 ___ 。
(3) 若混合物仍为 0.1mol ,其中镁粉的物质的量分数为 a ,用 100mL2mol·L -1 硫酸溶解此混合物后,再加入 450mL1mol·L -1 NaOH 溶液,所得沉淀中无 Al(OH) 3 ,写出满足此条件的 a 的取值范围: ____ 。
答案
(1) OH - +H + =H 2 O 、 Mg 2+ +2OH - =Mg(OH) 2 ↓ 、 Al 3+ +3OH - =Al(OH) 3 ↓ 、 Al(OH) 3 +OH - = +2H 2 O 0.06 440
(2)400
(3)0.5≤a < 1
【解析】
(1)
①O 点到 V 1 点说明为 H 2 SO 4 和 NaOH 反应。离子方程式为: OH - +H + =H 2 O , V 1 是开始生成沉淀,离子方程式为: Mg 2+ +2OH - =Mg(OH) 2 ↓ , Al 3+ +3OH - =Al(OH) 3 ↓ ,然后沉淀减少,是由于 Al(OH) 3 +OH - = +2H 2 O ,故在滴加 NaOH 溶液过程中有关反应的离子方程式为 OH - +H + =H 2 O 、 Mg 2+ +2OH - =Mg(OH) 2 ↓ 、 Al 3+ +3OH - =Al(OH) 3 ↓ 、 Al(OH) 3 +OH - =
+2H 2 O ,故答案为: OH - +H + =H 2 O 、 Mg 2+ +2OH - =Mg(OH) 2 ↓ 、 Al 3+ +3OH - =Al(OH) 3 ↓ 、 Al(OH) 3 +OH - =
+2H 2 O ;
② 当 V 1 =160mL 时,此时溶液是 MgSO 4 、 Al 2 (SO 4 ) 3 和 Na 2 SO 4 混合液,
由 Na + 离子守恒可知, n(Na 2 SO 4 )= n(Na + )=
n(NaOH)=
×0.16L×1mol/L=0.08mol ,设 MgSO 4 为 xmol , Al 2 (SO 4 ) 3 为 ymol ,则:根据 Mg 原子、 Al 原子守恒有: x+2y=0.1 ,根据
离子守恒有: x+3y=0.2-0.08 ,联立方程解得: x=0.06 、 y=0.02 ,所以金属粉末中 n(Mg)=0.06mol , n(Al)=2y=2×0.02mol=0.04mol ,滴加 NaOH 溶液到体积 V 2 时时,溶液是 Na 2 SO 4 和 NaAlO 2 混合液,根据 SO 4 2- 离子、 Na + 离子和 Al 原子守恒有: n(NaOH)=2n(Na 2 SO 4 )+n(NaAlO 2 )=2n(H 2 SO 4 )+n(Al)=2×0.1L×2mol/L×+0.04mol=0.44mol ,所以, V 2 =
=0.44L=440mL ,故答案为: 0.06 ; 440 ;
(2)
当溶液中 Mg 2+ 、 Al 3+ 恰好沉淀完全时,此时,溶液是 Na 2 SO 4 溶液,根据 离子和 Na + 离子守恒有: n(Na + )=2n(Na 2 SO 4 )=2(H 2 SO 4 )=2×0.1L×2mol/L=0.4mol ,所以, V(NaOH)=
=0.4L=400mL ,故答案为: 400 ;
(3)
若混合物仍为 0.1mol ,其中镁的物质的量分数为 a ,用 100mL 2mol•L -1 硫酸溶解后,再加入 450mL 1mol•L -1 氢氧化钠溶液,所得溶液无 Al(OH) 3 沉淀,证明生成的氢氧化铝全部和氢氧化钠反应,由上述分析知: v 1 =400ml ,再加入 50mL 1mol•L -1 氢氧化钠溶液,所得 Al(OH) 3 沉淀完全溶于氢氧化钠生成偏铝酸钠, Al(OH) 3 +NaOH=NaAlO 2 +2H 2 O , Al(OH) 3 最大取值 0.05mol ,即 0 < n(Al)≤0.05mol , n(Mg)+n(Al)=0.1mol ,则 0.5≤n(Mg) < 1 ,故答案为: 0.5≤a < 1 ;
