海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。请回答下列问题:
(1) 历史最久,技术和工艺也比较成熟,但成本较高的海水淡化方法是 _______ 。
(2) 步骤 1 中,粗盐中含有 、
、
等杂质离子,精制时常用的试剂有: ① 稀盐酸; ② 氯化钡溶液; ③ 氢氧化钠溶液; ④ 碳酸钠溶液。下列加入试剂的顺序正确的是 _______( 填字母 )
A . ①②③④ B . ②③④① C . ④③②① D . ③②④①
(3) 海水提溴工艺中热空气吹出 ,利用了溴的 _______ 性质;吹出的溴蒸气在吸收塔中被
和水吸收,写出离子方程式 _______ 。
(4) 为了把海水中 转化为
,从原料来源及经济效益角度考虑,最好选用 _______ 。
a. 氨水 b. 氢氧化钙 c. 氢氧化钠
(5) 写出无水氯化镁制备 Mg 的化学方程式: _______ 。
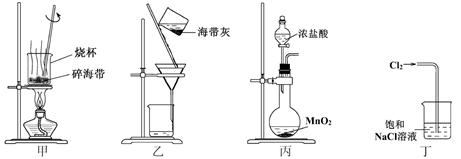
(6) 在实验室模拟海带提碘的实验过程。灼烧海带时,会用到的主要仪器有酒精灯、三脚架、玻璃棒、 _______ 。
答案
(1) 蒸馏
(2)B
(3) 挥发 SO 2 +Br 2 +2H 2 O=4H + +2Br - +SO
(4)b
(5)MgCl 2 ( 熔融 ) Mg+Cl 2 ↑
(6) 坩埚
【解析】
(1)
成本较高的海水淡化的方法是蒸馏法,因为蒸馏过程消耗大量的热能,故答案为:蒸馏;
(2)
精制时加入试剂的顺序为 ③ 氢氧化钠溶液,除去镁离子, ② 氯化钡溶液,除去硫酸根离子, ④ 碳酸钠溶液,除去过量的钡离子和钙离子,最后加入 ① 盐酸,除去过量的氢氧化钠和碳酸钠,其中 ③ 和 ② 的顺序可以颠倒,故顺序为 ③②④① 或 ②③④① ,故答案为: B ;
(3)
通入热空气或水蒸气吹出 Br 2 ,利用了溴的挥发性;溴蒸气在吸收塔中被 和水吸收生成 HBr 和硫酸,反应的离子方程式为: SO 2 +Br 2 +2H 2 O=4H + +2Br - +SO
,故答案为:挥发; SO 2 +Br 2 +2H 2 O=4H + +2Br - +SO
;
(4)
为使母液中的 MgCl 2 转化为 Mg(OH) 2 ,从原料来源及经济效益角度考虑,最好选用氢氧化钙,便宜易得,故答案为: b ;
(5)
电解熔融氯化镁反应生成氯气和镁,反应的化学方程式为: MgCl 2 ( 熔融 ) Mg+Cl 2 ↑ ;
(6)
固体灼烧需要坩埚,实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、坩埚等,故答案为:坩埚。