将质量和大小都完全相同的两份锌粒 a.b 分别加入过量且等体积等物质的量浓度的稀 ,同时向 a 的溶液中加入少量的
溶液,下列各图表示的是产生
的体积 V 与时间 t 的关系,其中正确的是
A . 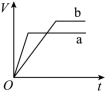 B .
B . 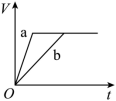 C .
C . 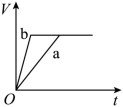 D .
D . 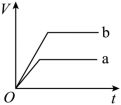
答案
A
【解析】
【详解】
锌和稀硫酸反应,加入硫酸铜,锌会和硫酸铜反应置换出金属铜,形成锌、铜、稀硫酸原电池,原电池反应加速金属锌和稀硫酸的反应,所以反应速率是: a>b ,速率越大,锌完全反应所用的时间越短,所以 a 所用的时间小于 b 的时间;锌过量的稀硫酸反应时,产生氢气的量取决于金属锌的质量, a 中金属锌一部分用于置换金属铜,导致和稀硫酸反应 生成氢气的量减少,所以产生氢气的体积 a 小于 b ,则符合变化的图示为 A ,故选 A 。



 B
B
 D
D