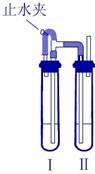
某铁的氧化物粉末可能含有 FeO 、 Fe 2 O 3 中的一种或两种。某化学兴趣小组同学利用以下装置测定铁的氧化物的组成,请协助完成,并回答有关问题。
(1) 李同学利用 1mol/L 的硫酸、 KSCN 溶液、新制氯水、酸性高锰酸钾溶液,确定其组成。
| 编号 | 实验操作 | 实验现象与结论 |
| ① | 取少量粉末放入试管中,注入的硫酸 | 粉末逐渐溶解,溶液呈黄绿色 |
| ② ③ | 将①中所得溶液分成两份,向其中一份滴加几滴溶液,振荡 向盛有 ___ 溶液的试管中滴加另一份溶液(填化学式) | 若溶液变为 ___ ,说明有 Fe 2 O 3 存在 若溶液 ____ ,说明有 FeO 存在 |
(2) 某兴趣小组同学查阅资料后获悉: H 2 C 2 O 4 CO↑+CO 2 ↑+H 2 O ,并拟用下列装置进行定量探究。

① 装置甲的作用是 ____ ;装置丁中的实验现象是 ______ 。
② 实验开始时发现打开分液漏斗旋塞,浓硫酸无法滴下,原因是 ___ 。
③ 若丙中铁的氧化物质量为 3.04g ,完全反应后丁中生成沉淀的质量为 9.85g 。试通过计算确定该铁的氧化物的成分中 FeO 、 Fe 2 O 3 的物质的量分别为 ____ 、 _____ 。
答案
血红色 KMnO 4 紫色褪去 除去 CO 2 出现白色沉淀 分液漏斗的玻璃塞没有打开 0.01mol 0.02mol
【分析】
根据图示装置及题给信息知, H 2 C 2 O 4 分解产生的气体有 CO 、 CO 2 、 H 2 O ,装置甲的作用是除去 CO 2 ,装置乙的作用是吸水,装置丙中是 CO 还原铁的氧化物,生成铁和 CO 2 , CO 2 能与 Ba ( OH ) 2 反应生成碳酸钡沉淀和水,据此分析解答。
【详解】
(1) ② Fe 3+ 遇到 KSCN 溶液,溶液变为血红色,若溶液变为血红色,则 “ ① ” 中溶液含有 Fe 3+ ,原固体中有 Fe 2 O 3 ,故答案为:血红色;
③ KMnO 4 溶液能氧化 Fe 2+ ,本身紫色褪去,若向另一份中加入少量 KMnO 4 溶液,紫色褪去,则 “ ① ” 中溶液含有 Fe 2+ ,原固体中有 FeO ,故答案为: KMnO 4 ;紫色褪去;
(2)① 根据 H 2 C 2 O 4 分解产生的气体有 CO 、 CO 2 、 H 2 O ,装置甲的作用是除去 CO 2 ,装置乙的作用是吸水,装置丙中是 CO 还原铁的氧化物,生成铁和 CO 2 , CO 2 能与 Ba(OH) 2 反应生成碳酸钡沉淀和水,故答案为:除去 CO 2 ;出现白色沉淀;
② 根据图示装置分析,分液漏斗的玻璃塞没有打开会出现浓硫酸无法滴下的情况,故答案为:分液漏斗的玻璃塞没有打开;
③CO 通过还原铁的氧化物会产生 CO 2 ,装置丁中的实验现象是变浑浊,产生白色沉淀:由 CO 2 +Ba(OH) 2 =BaCO 3 ↓ +H 2 O ,则 , n(CO 2 )=
,设 FeO 和 Fe 2 O 3 各有 amol , bmol ,则
,根据装置丙中的反应方程式中碳原子守恒得:
,联立解得 a=0.01 , b=0.02mol ,故答案为: 0.01mol ; 0.02mol 。