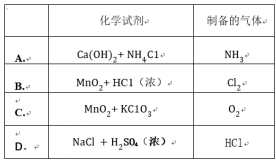
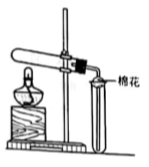
过渡金属元素铬( Cr )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用,回答下列问题:
( 1)对于基态 Cr原子,下列叙述正确的是_ ____(填标号 )。
A .轨道处于半充满时体系总能量低 , 核外电子排布应为 ![]() 3d 5 4s 1
3d 5 4s 1
B.4s电子能量较高,总是在比 3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
( 2)三价铬离子能形成多种配位化合物。 ![]() 中提供电子对形成配位键的原子是 _ ___,中心离子的配位数为 _ ____。
中提供电子对形成配位键的原子是 _ ___,中心离子的配位数为 _ ____。
(3) ![]() 中配体分子 N H 3 、 H 2 O以及分子 P H 3 的空间结构和相应的键角如下图所示。
中配体分子 N H 3 、 H 2 O以及分子 P H 3 的空间结构和相应的键角如下图所示。
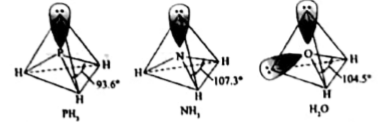
P H 3 中 P的杂化类型是_ _____, NH 3 的沸点比 PH 3 的 ______,原因是____。H 2 O的键角小于NH 3 的,分析原因 ______。
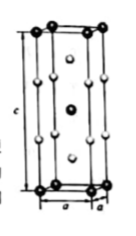
( 4)在金属材料中添加 Al Cr 2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 Al Cr 2 具有体心四方结构,如图所示。处于顶角位置的是 _ _____原子。设 Cr和Al原子半径分别为 和
,则金属原子空间占有率为 _______%(列出计算表达式)。
答案
(1)A C
(2)N O Cl , 6
(3) sp3 高
NH3分子间形成氢键增大分子间作用力,H2O分子有两对孤对电子,而NH3分子有一对孤对电子,所以H2O中孤对电子对键的斥力比NH3大,键角小
( 4)Al