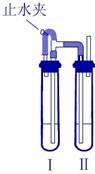
化合物 M 由两种元素组成,某研究小组按如下图流程探究其组成:
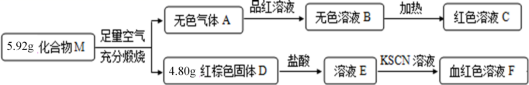
请回答:
(1) 溶液 E 的颜色是 _______ ,溶液 E 转化为溶液 F 的离子方程式是 _______ 。
(2) 化合物 M 的化学式为 _______ 。
(3) 化合物 M 在足量空气中充分煅烧的化学方程式为 _______ 。
(4) 将气体 A 通入溶液 E 中,其反应的离子方程式为 _______ 。
答案
黄褐色 Fe 3+ +3SCN - =Fe(SCN) 3 Fe 3 S 4 4Fe 3 S 4 +25O 2 6Fe 2 O 3 +16SO 2 2Fe 3+ +SO 2 +2H 2 O=2Fe 2+ +SO
+4H +
【分析】
化合物 M 由两种元素组成,在足量的空气中煅烧,生成的无色气体 A 能使品红溶液褪色,且加热时,溶液再次恢复,则气体 A 为二氧化硫;红棕色固体 D 溶于盐酸后,滴加 KSCN 溶液,溶液变红,则溶液 F 中含有铁离子,则固体 D 为氧化铁, 4.80g 时的物质的量为 0.03mol ,含有 Fe 元素的质量为 3.36g ,化合物 M 中含有 0.08mol S ,则化合物 M 的化学式为 Fe 3 S 4 。
【详解】
(1) 溶液 E 为氯化铁,则溶液的颜色为黄褐色;氯化铁与 KSCN 反应生成硫氰化铁和氯化钾,离子方程式是 Fe 3+ +3SCN - =Fe(SCN) 3 ;
(2) 分析可知,化合物 M 的化学式为 Fe 3 S 4 ;
(3) 化合物 M 为 Fe 3 S 4 ,在足量空气中充分煅烧生成氧化铁和二氧化硫,化学方程式为 4Fe 3 S 4 +25O 2 6Fe 2 O 3 +16SO 2 ;
(4) 气体 A 通入溶液 E 中,二氧化硫、水与铁离子反应生成硫酸根离子、氢离子和亚铁离子,反应的离子方程式为 2Fe 3+ +SO 2 +2H 2 O=2Fe 2+ +SO +4H + 。