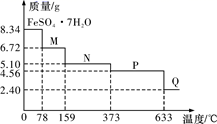
称取 CuO 和 Fe 2 O 3 的固体混合物 4.00 g ,加入 50.0 mL 2.00 mol/L 的 H 2 SO 4 充分反应,往所得溶液中加入 5.60 g Fe 粉,充分反应后,得到固体的质量为 3.04 g 。请计算:
(1) 加入 Fe 粉充分反应后,溶液中溶质的物质的量 _______ mol 。
(2) 固体混合物中 CuO 的质量分数 _______ 。
答案
0.1 95%
【详解】
过程发生的反应: ;
,充分反应后,得到固体质量为 3.04g ,则该固体为 Cu ,所以其物质的量为
,根据铜元素守恒,混合物中 CuO 的质量为
,所以 CuO 的质量分数
;加入铁粉充分反应后,溶液中的溶质为硫酸亚铁 (
) 溶液,根据硫酸根守恒可等得到
的物质的量为
,故答案为: 0.1mol ; 95% ;



 N2+3Cu+3H2O
N2+3Cu+3H2O