铁红 (Fe 2 O 3 ) 常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣 ( 主要成分为 Fe 2 O 3 、 Fe 3 O 4 ,另含少量难溶杂质 ) 为主要原料制备铁红的一种工艺流程如下
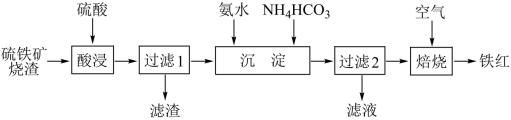
(1) 工业常将硫铁矿烧渣经过 ___________ 后再进行 “ 酸浸 ” 。
(2)“ 酸浸 ” 时加入的硫酸不宜过量太多的原因是 ___________ 。
(3)“ 沉淀 ” 完全后, ___________ ( 填操作 ) 一段时间,这样做方便过滤,减少杂质。
(4)“ 过滤 2” 所得滤渣若未洗涤充分,干燥后的主要成分为 FeOOH 和 FeCO 3 ,还有少量杂质是 ___________ ( 填化学式 ) 。
(5) 写出 FeCO 3 焙烧生成铁红的化学方程式: __________
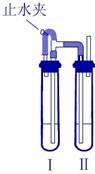
研究小组采用如下装置制取 FeCO 3 (C 后及夹持装置略 ) 。操作的关键是向 Na 2 CO 3 溶液 (pH=12.1) 通入一段时间 CO 2 至溶液 pH 为 7 ,再滴加一定量 FeSO 4 溶液,产生白色沉淀。
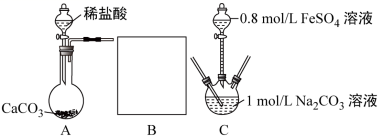
(6)B 中所用试剂为 __________ ;
A .浓硫酸 B .饱和碳酸钠 C .饱和碳酸氢钠 D .饱和食盐水
(7) 先向 1mol/LNa 2 CO 3 溶液中通入 CO 2 的目的是 __________
(8)a 克粗品 FeCO 3 ( 杂质不含铁元素 ) 在空气中焙烧后剩余固体质量为 b 克,假设 FeCO 3 全部生成三氧化二铁,则粗品 FeCO 3 中 FeCO 3 的纯度为 __________ 。
答案
粉碎 过量太多会增加沉淀过程氨水的用量 煮沸 (NH 4 ) 2 SO 4 4FeCO 3 + O 2 2Fe 2 O 3 + 4CO 2 c 排空气,防止亚铁被氧化,降低 OH - 的浓度,防止生成 Fe(OH) 2
【分析】
硫铁矿烧渣(主要成分为 Fe 2 O 3 、 Fe 3 O 4 ,另含少量难溶杂质)加入足量硫酸, Fe 2 O 3 、 Fe 3 O 4 与酸反应生成的硫酸亚铁、硫酸铁;,在滤液中加入氨水、碳酸氢铵调节 pH 值,得到 FeOOH 和 FeCO 3 ,在空气中焙烧,发生 4FeCO 3 + O 2 2Fe 2 O 3 + 4CO 2 ,生成氧化铁和二氧化碳,同时 FeOOH 生成 Fe 2 O 3 ,
【详解】
(1)“ 酸浸 ” 前将硫铁矿烧渣经过粉碎,可增大反应物接触面积,加快反应速率,提高烧渣浸出率,故答案为:粉碎;
(2) 当氨水用量超过一定体积时,铁的沉淀率下降,可能原因是氨水与铁的氢氧化物反应生成可溶性配合物,故答案为:过量太多会增加沉淀过程氨水的用量;
(3) 为方便过滤,沉淀完全后,需要进行的操作是煮沸一段时间有利于沉淀凝聚紧密,获得紧密颗粒的沉淀,方便过滤,故答案为:煮沸;
(4) 在过滤之前的流程中加入过量的硫酸中有 ,还加入氨水和 NH 4 HCO 3 引入
,且
和
均未转化为沉淀而留在滤液中,故主要溶质为 (NH 4 ) 2 SO 4 ,则 “ 过滤 2” 所得滤渣干燥后的主要成分为 FeOOH 和 FeCO 3 ,还有少量杂质是 (NH 4 ) 2 SO 4 ;故答案为: (NH 4 ) 2 SO 4 ;
(5)FeCO 3 在空气中焙烧生成铁红的化学方程式为 4FeCO 3 + O 2 2Fe 2 O 3 + 4CO 2 。
(6) 装置 A 反应制得的 CO 2 气体中含有氯化氢气体,影响后续制取实验,通入 C 装置前应先进行洗气除杂,所以装置 B 中装有饱和碳酸氢钠,故答案为: C ;
(7) 装置中含有空气,空气中的氧气可以将亚铁离子氧化为铁离子, CO 2 可将装置中的氧气排除,防止亚铁离子氧化;同时碳酸钠溶液碱性强,溶液中 c(OH - ) 大,就会出现生成氢氧化亚铁与制备的 FeCO 3 成为竞争反应,而导致制备的 FeCO 3 纯度低, NaHCO 3 溶液碱性弱,制得 FeCO 3 纯度高,则先向 1mol/LNa 2 CO 3 溶液中通入 CO 2 的目的是排除装置中的空气,降低溶液中 OH - 的浓度,防止生成 Fe(OH) 2 ,故答案为:排空气,防止亚铁被氧化,降低 OH - 的浓度,防止生成 Fe(OH) 2 ;
(8) 设 FeCO 3 的质量为 x , ,解得
,则粗品 FeCO 3 中 FeCO 3 的纯度为
。