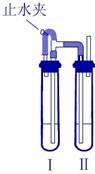
FeCO 3 是制备补血剂原料之一、实验室里制备 FeCO 3 的流程如下图所示:
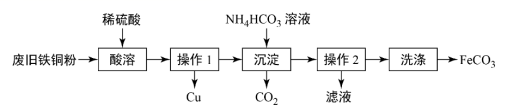
回答下列问题:
(1)“ 酸溶 ” 时,常采取加热或搅拌措施,其原因是 _______ 。
(2)“ 操作 1” 和 “ 操作 2” 需用的玻璃仪器有 _______ 。
(3) 写出 “ 沉淀 ” 时反应的化学方程式 _______ 。
(4)“ 沉淀 ” 反应前,检验溶液中是否含有 Fe 2+ ,应选用的试剂是 _______ 。
(5) 检验是否 “ 洗涤 ” 干净的方法是 _______ 。
答案
加快酸溶的速率 烧杯、漏斗、玻璃棒 铁氰化钾(其他合理答案亦可) 取最后一次洗涤液,加适量盐酸酸化后滴入氯化钡溶液,若未出现白色沉淀,则沉淀洗涤干净
【分析】
向废铁铜粉中加入过量硫酸,混合物中的铁与硫酸反应生成硫酸亚铁,而硫酸不与铜反应,则用过滤法可将其除去;然后向滤液中加入过量的碳酸氢铵溶液沉淀亚铁离子;然后再过滤洗涤得到碳酸亚铁,据此分析可得;
【详解】
(1) 加热或搅拌能加快化学反应速率,提高单位时间内的浸出率,所以 “ 酸溶 ” 时,常采取加热或搅拌措施,其目的是加快酸溶的速率,故答案为:加快酸溶的速率;
(2)“ 操作 1” 和 “ 操作 2” 均为分离难溶性固体和可溶性的物质,所选方法为过滤。过滤所需的玻璃仪器有:烧杯、漏斗、玻璃棒,故答案为:烧杯、漏斗、玻璃棒;
(3)“ 沉淀 ” 时为碳酸氢铵和硫酸亚铁反应生成碳酸亚铁沉淀、硫酸铵、水和二氧化碳,则 ,故答案为:
;
(4)“ 沉淀 ” 反应前,取适量样品于一支洁净的试管中,然后向试管中滴入数滴铁氰化钾溶液,若有蓝色沉淀生成,则样品中含亚铁离子,故答案为:铁氰化钾(其他合理答案亦可);
(5) 从反应 可知,沉淀表面硫酸铵,那么检验沉淀是否 “ 洗涤 ” 干净的方法是:取最后一次洗涤液,加适量盐酸,无明显现象,后滴入氯化钡溶液,若未出现白色沉淀,则沉淀洗涤干净,故答案为:取最后一次洗涤液,加适量盐酸,无明显现象,后滴入氯化钡溶液,若未出现白色沉淀,则沉淀洗涤干净。