以红土镍矿 ( 主要含有 Fe 2 O 3 、 FeO 、 NiO 、 SiO 2 等 ) 为原料,获取净水剂黄钠铁矾 ![]() 和纳米镍粉的部分工艺流程如图:
和纳米镍粉的部分工艺流程如图:
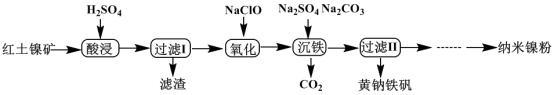
已知: Fe 3+ 在 pH 约为 3.7 时可完全转化为 Fe(OH) 3 , Fe 2+ 在 pH 约为 9 时可完全转化为 Fe(OH) 2
下列说法错误的是 ( )
A . “ 滤渣 ” 的主要成分是 SiO 2
B . 为提高镍、铁元素的利用率,可将 “ 过滤 I” 的滤液和滤渣洗涤液合并
C . “ 氧化 ” 过程发生的离子方程式为 2H + +2Fe 2+ +ClO - =2Fe 3+ +Cl - +H 2 O
D . “ 沉铁 ” 过程中加入碳酸钠的作用是调节溶液的酸碱度,应将 pH 控制在 3.7~9
答案
D
【分析】
红土镍矿 ( 主要含有 Fe 2 O 3 、 FeO 、 NiO 、 SiO 2 等 ) 中加入硫酸酸浸,酸浸后的酸性溶液中含有 Ni 2+ 、 Fe 2+ 、 Fe 3+ 等,二氧化硅不溶,形成滤渣,滤液中加入 NaClO 氧化亚铁离子为铁离子,再加入碳酸钠溶液调节溶液的 pH ,使铁离子全部沉淀,过滤后得到沉淀黄钠铁矾,滤液经处理可得到 Ni ,据此分析解答。
【详解】
A .根据上述分析,二氧化硅不溶于硫酸,形成滤渣,故 A 正确;
B .滤渣表面吸附有滤液中的镍、铁元素,为提高镍、铁元素的利用率,可将 “ 过滤 I” 的滤液和滤渣洗涤液合并,故 B 正确;
C . “ 氧化 ” 过程中 NaClO 氧化 Fe 2+ 生成 Fe 3+ ,反应的离子方程式为 2H + +2Fe 2+ +ClO - =2Fe 3+ +Cl - +H 2 O ,故 C 正确;
D . Fe 3+ 在 pH 约为 3.7 时可完全转化为 Fe(OH) 3 , Fe 2+ 在 pH 约为 9 时可完全转化为 Fe(OH) 2 , “ 沉铁 ” 过程中加入碳酸钠的作用是调节溶液的酸碱度形成黄钠铁矾 ![]() ,应将 pH 控制在 pH < 3.7 ,故 D 错误;
,应将 pH 控制在 pH < 3.7 ,故 D 错误;
故选 D 。