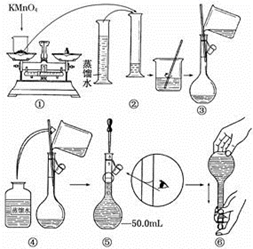
配制一定物质的量浓度的溶液,几个关键实验步骤和操作如图:
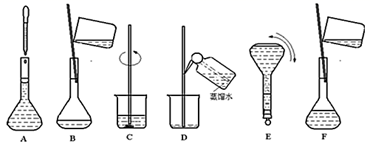
(1) 现需要 94 mL 0.10 mol·L - 1 Na 2 CO 3 溶液,进行现场配制。上述实验步骤 A~F 正确的实验次序为 _______________________ ( 填字母 ) 。步骤 E 中将一玻璃仪器上下颠倒数次,写出该仪器的名称 _________________ 。
(2) 步骤 C 通常称为溶解,步骤 A 通常称为 _________ 。
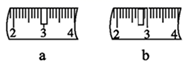
(3) 用 Na 2 CO 3 ·10H 2 O 来配制该溶液,托盘天平称取样品,游码需要打在图示 ________ ( 填 a 或 b) 位置,若称量前晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏 _______ ( 填 “ 大 ” 或 “ 小 ” 或 “ 无影响 ”) 。
答案
CBDFAE 100 mL 容量瓶 定容 a 大
【分析】
本题考察一定物质的量浓度溶液配制,难度不大,考生运用所学知识答题即可。
【详解】
( 1 )配制一定物质的量浓度溶液的操作步骤为 : 计算 → 称量 → 溶解 → 移液 → 洗涤 → 定容 → 摇匀 → 装瓶;上述实验步骤中, A 为定容, B 为移液, C 为溶解, D 为洗涤, E 为摇匀, F 为洗涤后的加水,故正确的实验次序为 CBDFAE ; E 为容量瓶,由于要配制 94mL 的溶液,需要使用 100mL 的规格,故 E 为 100mL 容量瓶;
( 2 ) A 为定容;
( 3 )实验需要使用 100mL 容量瓶,则 n(Na 2 CO 3 ·10H 2 O)=0.1L×0.1mol·L -1 =0.01mol , m(Na 2 CO 3 ·10H 2 O)=0.01mol×286g·mol -1 =2.9g ,则需要用游码称 0.9g ,故选 a ;称量前晶体已经有一部分失去了结晶水,则称得的晶体中 n(Na 2 CO 3 ) 偏大,故所配制的溶液浓度偏大。