Ⅰ .实验室需要 480mL 物质的量浓度为 0.1mol/L 的 KMnO 4 溶液,回答问题:
(1) 要配制上述溶液,所需仪器除天平、药匙、烧杯、玻璃棒、胶头滴管外,还需要 _______ ;
(2) 根据计算,需称量 KMnO 4 固体的质量为 ______ g ;
(3) 下列操作会导致所配溶液浓度 偏低 的是 _____ ( 填选项代号 ) 。
A .定容时加水超过刻度线,用胶头滴管吸出一些
B .定容时仰视刻度线
C .转移溶液后,没有洗涤烧杯内壁
D .配制前容量瓶内壁仍残留有蒸馏水
E .转移溶液时部分溶液溅出
Ⅱ . KMnO 4 是一种强氧化剂, 加酸酸化能够提高其氧化性,通常用硫酸酸化而不能用盐酸酸化,原因是 KMnO 4 可以和盐酸发生反应。
(4) 用双线桥法分析反应: 2 +10Cl - +16H + =2Mn 2+ +5Cl 2 ↑+8H 2 O 。 _____ ,该反应中,还原产物是 _____ 。判断氧化剂和氧化产物的氧化性强弱 _______ 。
(5) 若转移的电子数为 0.4mol ,则产生标况下气体体积为 __________ 。
答案
500mL 容量瓶 7.9g ABCE 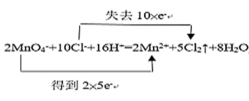 Mn 2+
Mn 2+ 大于 Cl 2 4.48L
【分析】
配制步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作;根据氧化还原反应规律进行分析:该反应中 10e - ~5Cl 2 关系进行计算。
【详解】
(1) 实验室需要 480mL 物质的量浓度为 0.1mol/L 的 KMnO 4 溶液需要使用 500mL 容量瓶,配制步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般天平称量固体,把高锰酸钾倒入烧杯进行溶解,冷却后转移到 500mL 容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线 1 ~ 2cm 时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、天平、药匙、烧杯、胶头滴管、 500mL 容量瓶;
(2) 的物质的量为
,
的质量为
;
(3) 根据 c = 分析;
A .定容时加水超过刻度线,用胶头滴管吸出一些,导致溶质的物质的量偏小,配制的溶液浓度偏低,故 A 符合题意;
B .定容时仰视,导致溶液的体积偏大,所以配制溶液的浓度偏低,故 B 符合题意;
C .转移溶液后,没有洗涤烧杯内壁,导致溶质的物质的量偏小,配制的溶液浓度偏低,故 C 符合题意;
D .配制前容量瓶内壁仍残留有蒸馏水,对溶质的物质的量和溶液的体积无影响,所以配制的溶液浓度无影响,故 D 不符合题意;
E .转移溶液时部分溶液溅出容量瓶外,导致溶质的物质的量偏小,配制的溶液浓度偏低,故 E 符合题意;
故答案为: ABCE ;
(4)2 +10Cl - +16H + =2Mn 2+ +5Cl 2 ↑+8H 2 O ,该反应中锰元素化合价从 +7 价降低到 +5 价,两个锰原子的化合价降低,得 2×5e - 电子,高锰酸根作氧化剂;氯元素化合价从 -1 价升高到 0 价, 10 个氯原子失 10×e - 电子,氯离子作还原剂;锰离子是化合价降低后得到的还原产物,氯气是化合价升高后得到的产物是氧化产物;故双线桥为:
 ,还原产物是化合价降低后得到的产物,即 Mn 2+ ,由于氧化剂的氧化性强于氧化产物,故氧化性:
,还原产物是化合价降低后得到的产物,即 Mn 2+ ,由于氧化剂的氧化性强于氧化产物,故氧化性: 大于 Cl 2 ;
(5)2 +10Cl - +16H + =2Mn 2+ +5Cl 2 ↑+8H 2 O ,锰元素的化合价从 +7 降低到 +2 价,两个锰原子的化合价降低,氯元素的化合价从 -1 价升高到 0 价, 10 个氯原子的化合价升高;该反应转移了 10 个电子,即转移 10 个电子生成 5 个氯气分子,故转移 0.4mol 电子时生成氯气 0.2mol ,根据 V = nV m=0.2mol×22.4L/mol=4.48L 。
