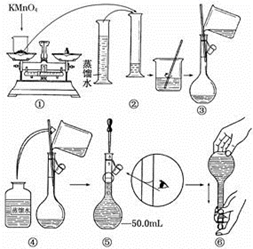
下面是用 36.5% 的浓盐酸 (ρ=1.18g/cm 3 ) 配制成 1mol/L 的稀盐酸 500mL 的操作,请按要求填空:
(1) 所需浓盐酸的体积为 _____ mL( 保留一位小数 ) 。
(2) 如果实验室应选用 _________ mL 量筒最好。
(3) 将量取的浓盐酸沿烧杯内壁慢慢注入盛有约 200mL 水的烧杯里,并不断搅拌。
(4) 将冷却至室温的上述溶液沿玻璃棒注入 ______________ 中,并用 50mL 蒸馏水洗涤烧杯 2 ~ 3 次,洗涤液要注入上述仪器中,并摇匀。
(5) 加水至距刻度 1 ~ 2cm 时,改用胶头滴管加水,使溶液的凹液面正好跟刻度相平。
(6) 误差分析:请用 “ 偏高 ”“ 偏低 ” 或 “ 无影响 ” 进行填空
①定容时,观察液面俯视,则浓度 _____ ,
②定容时,水加多了,用滴管吸出,则浓度 _____ 。
答案
42.4 50 500 mL 容量瓶 偏高 偏低
【详解】
36.5% 的浓盐酸 (ρ=1.18 g/cm 3 ) 的物质的量浓度为 = 11.8 mol/L 。
(1) 用浓溶液配制稀溶液的过程中,溶质的物质的量相同,设所需浓盐酸的体积为 V ,则有: V×11.8 mol/L = 0.5 L×1 mol/L ,解得 V = 0.04237 L≈42.4 mL 。
(2) 用量筒量取液体时,尽可能减少量取次数,因而选用大而相近量程的量筒最好,根据计算结果,此处选用 50 mL 量筒最好。
(4) 实验要求配制 500 mL 溶液,故选用 500 mL 容量瓶。待冷却至室温后,将溶液沿玻璃棒注入 500 mL 容量瓶中。
(6)① 定容时,观察页面俯视会造成读数偏大,即所加水体积低于刻度线,溶液体积偏小,浓度偏高; ② 定容时,水加多了,用滴管吸出,部分溶质被吸出,即所得溶液中溶质减少,所配溶液物质的量浓度偏低。