钠、碳及它们的化合物在生产、生活中有着重要的用途。
(1) 某汽车安全气囊的产气药剂主要含有 NaN 3 、 Fe 2 O 3 、 KClO 4 、 NaHCO 3 等物质。当汽车发生碰撞时, NaN 3 迅速分解产生 N 2 和 Na ,同时放出大量的热。 N 2 使气囊迅速膨胀,从而起到保护作用。
① KClO 4 的名称是 ___________ ,具有 ___________ ( 填 “ 还原性 ” 或 “ 氧化性 ”) 。
② Fe 2 O 3 可处理产生的 Na ,反应为 6Na+Fe 2 O 3 =3Na 2 O+2Fe ,反应中 Na 作 ___________ ( 填 “ 还原剂 ” 或 “ 氧化剂 ”) 。
反应过程中氧化产物与还原产物的个数比为: ___________ 。
(2)Na 2 O 2 可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究 Na 2 O 2 与 CO 2 的反应。请回答下列问题:
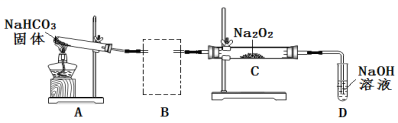
①根据实验目的,虚线框中的装置所用的试剂为 ___________ 。
②装置 C 中观察到的现象是 ___________ ,反应的化学方程式是 ___________ 。
③装置 A 的作用是制备 CO 2 ,写出 A 中发生反应的化学方程式是 ___________ 。
答案
高氯酸钾 氧化性 还原剂 3 : 2 浓硫酸 固体由淡黄色变为白色 2CO 2 +2Na 2 O 2 =2Na 2 CO 3 +O 2 2NaHCO 3 Na 2 CO 3 +H 2 O+CO 2 ↑
【详解】
(1) ①在 KClO 4 中 Cl 元素化合价为 +7 价,是高氯酸的钾盐,名称是高氯酸钾;该物质是 Cl 元素最高化合价的盐,只能得到电子,表现强的氧化性;
② Fe 2 O 3 可处理产生的 Na ,反应为 6Na+Fe 2 O 3 =3Na 2 O+2Fe ,在该反应中, Na 元素化合价升高,失去电子被氧化,所以 Na 作还原剂,氧化产物是 Na 2 O ; Fe 2 O 3 中的 Fe 得到电子,化合价降低,被还原, Fe 2 O 3 作氧化剂,还原产物是 Fe ,根据电子守恒可知:反应过程中氧化产物与还原产物的个数比为 3 : 2 ;
(2) ① NaHCO 3 不稳定,受热分解产生 Na 2 CO 3 、 H 2 O 、 CO 2 ,为探究 Na 2 O 2 与 CO 2 的反应,应该先除去装置中的水,但不吸收 CO 2 ,所以 B 为干燥装置,使用试剂是浓硫酸;
②在 C 中 CO 2 与 Na 2 O 2 反应产生 Na 2 CO 3 、 O 2 ,反应方程式为: 2CO 2 +2Na 2 O 2 =2Na 2 CO 3 +O 2 ;
③在装置 A 中 NaHCO 3 不稳定,受热分解产生 Na 2 CO 3 、 H 2 O 、 CO 2 ,故 A 的作用是制备 CO 2 ,则 A 中发生反应的化学方程式是: 2NaHCO 3 Na 2 CO 3 +H 2 O+CO 2 ↑ 。


