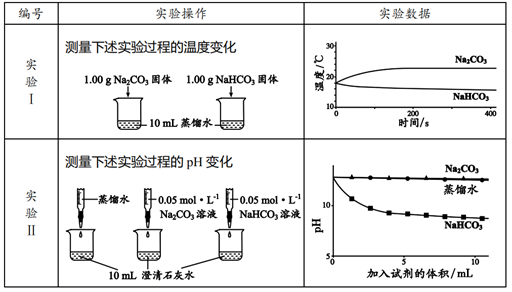
下列实验方案中,能测定 和
混合物中
质量分数的实验方案是 ( )
①仅 ag 混合物与过量氢氧化钠溶液充分反应,加热、蒸干、灼烧,得 bg 固体
②仅 ag 混合物充分加热后,固体质量减重 bg
③仅 ag 混合物与过量稀硫酸充分反应,逸出气体用碱石灰吸收,增重 bg
④仅 ag 混合物与过量 溶液充分反应,过滤、洗涤、干燥,得 bg 固体
⑤仅 ag 混合物与过量稀盐酸充分反应,加热、蒸干、灼烧,得 bg 固体
A . ②④⑤ B . ①②③④⑤ C . ②③④⑤ D . ①②④⑤
答案
A
【详解】
①取 ag 混合物与过量氢氧化钠溶液充分反应,加热、蒸干、灼烧,得 bg 固体, bg 固体为碳酸钠及过量 NaOH ,无法计算,故不选;
②只有碳酸氢钠加热分解,取 ag 混合物充分加热后,固体质量减重 bg ,可以用差量法计算其质量及质量分数,故选;
③取 ag 混合物与过量稀硫酸充分反应,逸出气体用碱石灰吸收,增重 bg , bg 为二氧化碳及水蒸气的质量,无法计算二氧化碳的质量,所以无法计算 Na 2 CO 3 或 NaHCO 3 的质量,不能测定混合物中 NaHCO 3 质量分数,故不选;
④取 ag 混合物与过量 Ba(OH) 2 溶液充分反应,过滤、洗涤、干燥,得 bg 固体, b 为碳酸钡的质量,由根据质量可列方程组计算固体中碳酸钠、碳酸氢钠的质量,可以测定混合物中 NaHCO 3 质量分数,故选;
⑤取 ag 混合物与过量稀盐酸充分反应,加热、蒸干、灼烧,得 bg 固体, bg 为 NaCl 质量,通过固体质量差利用差量法即可计算出 NaHCO 3 质量,可以测定混合物中 NaHCO 3 质量分数,故选;故 A 正确。
故选 A 。