KIO 3 是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO 3 的化学名称是 ___________________________________ 。
(2) 利用 “KClO 3 氧化法 ” 制备 KIO 3 工艺流程如下图所示:
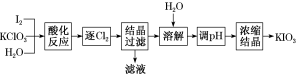
“ 酸化反应 ” 所得产物有 KH(IO 3 ) 2 、 Cl 2 和 KCl 。 “ 逐 Cl 2 ” 采用的方法是 _______________________________ 。 “ 滤液 ” 中的溶质主要是 ____________ 。 “ 调 pH” 中发生反应的化学方程式为 ___________________________________ 。
答案
碘酸钾 加热 KCl KH(IO 3 ) 2 + KOH=2KIO 3 + H 2 O( 或 HIO 3 + KOH=KIO 3 + H 2 O)
【分析】
酸化反应 ” 所得产物有 KH(IO 3 ) 2 、 Cl 2 和 KCl , Cl 2 的溶解度随温度的升高而降低,所以可以用加热的方法来达到 “ 逐 Cl 2 ” 的目的,滤液中的溶质主要是 KCl ,加入 KOH 调节 pH ,使 KH(IO 3 ) 2 转化为 KIO 3 ,据此解题。
【详解】
(1)KIO 3 的化学名称为碘酸钾。
(2)Cl 2 的溶解度随温度的升高而降低,所以可以用加热的方法来达到 “ 逐 Cl 2 ” 的目的; KH(IO 3 ) 2 和 KCl 的分离可以根据溶解度的不同,采用结晶法分离,滤液中的溶质主要是 KCl ,要使 KH(IO 3 ) 2 转化为 KIO 3 ,可以加入 KOH 调节 pH ,发生反应: KH(IO 3 ) 2 + KOH=2KIO 3 + H 2 O 或 HIO 3 + KOH=KIO 3 + H 2 O ,从而避免引入新的杂质离子。




 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。  2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。  HCl+HClO
HCl+HClO