某学习小组利用如图所示装置将氯气和空气 ( 不参与反应 ) 以体积比约为 1 : 3 混合后,与湿润的碳酸钠反应制取 Cl 2 O ,并进一步制取次氯酸。
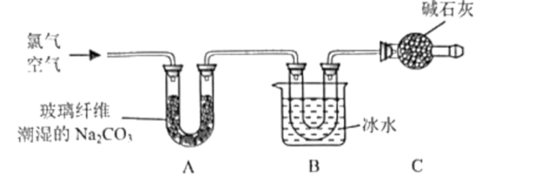
已知: Cl 2 O 是黄棕色具有强烈刺激性气味的气体,沸点为 2.2 ℃,易溶于 CC1 4 和水。其爆炸极限为 23.5%~100% ,与有机物、还原剂接触或加热时会燃烧或爆炸。
回答下列问题:
(1) 装置 C 的仪器名称为 ______ ,该装置的作用是 ______ 。
(2) 装置 A 中发生反应的化学方程式为 _______ 。
(3) 针对此实验的有关说法正确的是 _______ ( 填标号 ) 。
a. 装置不用橡胶管连接且橡胶塞要作保护处理,是为了防止橡胶燃烧或爆炸
b. 可利用 CCl 4 除去 Cl 2 O 中混有的 Cl 2
c. 氯气与空气混合的目的是将生成的 Cl 2 O 稀释,降低爆炸危险
(4) 为了进一步制取 HClO ,可将 Cl 2 O 通入水中,该过程宜在避光条件下进行,原因是 ______ ( 用化学方程式表示 ) ;此方法相较于用氯气直接溶于水制备次氯酸溶液的优点是 ______ ( 答出一条即可 ) 。
(5) 将制得的 HClO 溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能是 ① NaOH 被 HClO 中和; ② ______ 。设计实验探究溶液红色褪去的原因 ______ 。
答案
球形干燥管 吸收尾气 2Cl 2 +Na 2 CO 3 =Cl 2 O +2NaCl+CO 2
ac 2HClO
2HCl+O 2 ↑ 制取的次氯酸浓度较大 HClO 有漂白性 往褪色后的溶液中继续滴加氢氧化钠溶液,若溶液变红,证明褪色的原因为 ①;若溶液不显红色,证明褪色的原因为②
【详解】
(1) 干燥管;吸收未反应的氯气,防治污染空气,还可以防止空气中的水蒸气进入 B 中;
(2)A 中氯气与碳酸钠反应生成 Cl 2 O , 2Cl 2 +Na 2 CO 3 =Cl 2 O +2NaCl+CO 2
;
(3)a . Cl 2 O 具有强氧化性,与有机物、还原剂接触会燃烧或爆炸, a 正确; b. Cl 2 O 易溶于四氯化碳, b 错误; c. 氯气与空气混合稀释 Cl 2 O ,降低爆炸危险, c 正确;
(4) HClO 见光易分解,因此要避光, 2HClO 2HCl+O 2 ↑ ;方法相较于用氯气直接溶于水制备次氯酸溶液的优点是制取的次氯酸浓度较大、无副产物等;
(5) HClO 具有漂白性,使酚酞变色,可以设计实验为往褪色后的溶液中继续滴加氢氧化钠溶液,若溶液变红,证明褪色的原因为 ①;若溶液不显红色,证明褪色的原因为②。



 N2+3Cu+3H2O
N2+3Cu+3H2O