如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中 E 瓶放有干燥红色布条; F 中为红色的铜网,其右端出气管口放有脱脂棉。
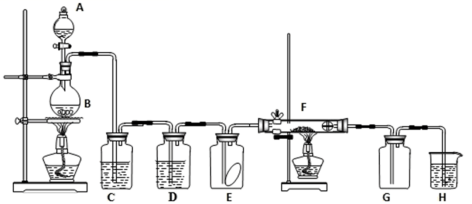
(1) 装置 C 中盛装的溶液是 _______ , D 中试剂的作用是 _______ 。
(2)E 中的红色布条是否褪色? _______ ( 填 “ 是 ” 或 “ 否 ”) 。
(3)H 中的试剂为 _______ ,用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,该反应的化学方程式为 _______ 。
答案
饱和氯化钠溶液 干燥氯气 否 氢氧化钠溶液 ( 或 NaOH 或强碱溶液 ) 2Cl 2 + 2Ca(OH) 2 =CaCl 2 + Ca(ClO) 2 + 2H 2 O
【分析】
实验室用浓盐酸和二氧化锰加热制取了氯气的反应,反应原理为 MnO 2 +4HCl( 浓 ) MnCl 2 +Cl 2 ↑ +2H 2 O ,实验装置中,最左侧为反应装置, C 、 D 为除杂装置, E 、 F 分别为检验 Cl 2 的漂白性和氧化性的装置, G 为收集装置, H 为尾气处理装置。
【详解】
(1) 实验室用浓盐酸和二氧化锰加热制取了氯气的反应,因为浓盐酸具有挥发性,制得气体中含有氯化氢和水蒸气,可用饱和食盐水除去氯化氢,用浓硫酸除去水蒸气,则装置 C 中盛装的溶液是饱和 NaCl 溶液,装置 D 中盛装的浓硫酸,用来干燥氯气,故答案为:饱和 NaCl 溶液;干燥氯气;
(2) 因为干燥的氯气不具有漂白性,所以红色布条不会褪色,故答案为:否;
(3) 因为氯气能和碱液反应,所以实验室用 NaOH 溶液来吸收多余氯气;氯气与氢氧化钙反应制得漂白粉,方程式为: 2Cl 2 + 2Ca(OH) 2 =CaCl 2 + Ca(ClO) 2 + 2H 2 O ,故答案为:氢氧化钠溶液 ( 或 NaOH 或强碱溶液 ) ; 2Cl 2 + 2Ca(OH) 2 =CaCl 2 + Ca(ClO) 2 + 2H 2 O 。




 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。  2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。  HCl+HClO
HCl+HClO