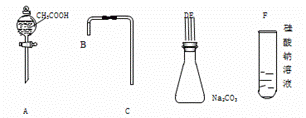
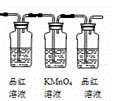
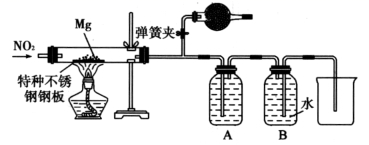
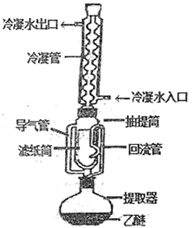
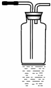ClO 2 又称百毒净,可用于水的净化和纸张、纺织品的漂白。用如下图所示装置 ( 夹持装置和加热装置省略 ) 制备 ClO 2 并探究 ClO 2 的某某些性质。

已知: ① 高氯酸:沸点 90 °C ,浓度低于 60% 比较稳定,浓度高 60% 遇含碳化合物易爆炸。
② 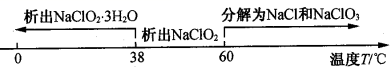
回答下列问题:
(1) (1) 仪器 a 的名称为 ___________ 。
(2) 补全并配平装置 A 制备 ClO 2 的化学方程式: ___________
_ _____NaClO 3 + ______H 2 SO 4 ( 浓 )= ______HClO 4 + ______ClO 2 +______NaHSO 4 +______
(3) 关闭止水夹 ② ,打开止水夹 ①③ ,通空气段时间后,装置 C 中生成 NaClO 2 ,离子方程式为 ___________ 。若关闭止水夹 ③ ,打开止水夹 ② , B 中可观察到的现象为 ___________ 。
(4) ) 从装置 C 反应后的溶液中获得 NaClO 2 晶体,常采用减压蒸发结晶。采用减压蒸发的原因是 ___________ ,减压蒸发时,当有较多晶体析出时,再 ___________ ( 填操作方法 ) ,洗涤,干燥即可得到 NaClO 2 。
(5) 城市饮用水处理,新技术用 NaClO 2 、 Na 2 FeO 4 替代 Cl 2 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么 NaClO 2 、 Na 2 FeO 4 、 Cl 2 三种消毒杀菌剂的消毒效率由大到小的排列顺序是 ___________ 。
答案
三颈烧瓶 : 3 3 1 2 3 1 2ClO 2 + 2OH — + H 2 O 2 =2ClO + 2H 2 O + O 2 红色布条褪色 减压可降低沸点,较低温度下蒸发,避免晶体高温分解 过滤 NaClO 2 >Cl 2 > Na 2 FeO 4
【分析】
A 装置由过量浓硫酸和氯酸钠反应制备二氧化氯和高氯酸,反应为 3NaClO 3 + 3H 2 SO 4 ( 浓 )=HClO 4 + 2ClO 2 ↑ + 3NaHSO 4 + H 2 O ,高氯酸遇含碳化合物易爆炸,故胶塞和导管接口必须包锡箔纸,关闭止水夹 ②,打开止水夹①③,通空气一段时间,二氧化氯和氢氧化钠和过氧化氢在 C 中反应: 2ClO 2 + 2OH — + H 2 O 2 =2ClO 2 — + 2H 2 O + O 2 ,控制温度 38 ℃~ 60 ℃下进行减压蒸发结晶可得晶体 NaClO 2 ,关闭止水夹 ③,打开止水夹②,二氧化氯有强氧化性,使 B 中红布条褪色,用 D 中氢氧化钠溶液吸收尾气,据此分析作答。
【详解】
(1) 仪器 a 为三颈烧瓶,由题可知,高氯酸浓度高于 60% 遇含碳化合物易爆炸,橡胶是含碳化合物,若生成的高氯酸浓度高时遇橡胶塞及导管易发生爆炸;故答案为:三颈烧瓶;
(2)A 种过量浓硫酸和 NaClO 3 反应制备二氧化氯和高氯酸,反应为 3NaClO 3 + 3H 2 SO 4 ( 浓 )=HClO 4 + 2ClO 2 ↑ + 3NaHSO 4 + H 2 O ;故答案为: 3 3 1 2 3 1 ;
(3) 关闭止水夹 ②,打开止水夹①③,二氧化氯和氢氧化钠和过氧化氢在 C 中反应, 2ClO 2 + 2OH — + H 2 O 2 =2ClO + 2H 2 O + O 2 ,若关闭止水夹 ③,打开止水夹②,二氧化氯有强氧化性,使 B 中红色布条褪色;故答案为: 2ClO 2 + 2OH — + H 2 O 2 =2ClO
+ 2H 2 O + O 2 ;红色布条褪色;
(4) 根据已知,温度低于 38℃ ,得到的晶体含有结晶水,温度高于 60℃NaClO 2 会分解,故从装置 C 反应后的溶液中获得晶体,需要控制温度在 38℃ ~ 60℃ 进行减压蒸发结晶,然后过滤、洗涤干燥得到 NaClO 2 ,采用减压蒸发的原因是减压可降低沸点,较低温度下蒸发,避免晶体高温分解;故答案为:减压可降低沸点,较低温度下蒸发,避免晶体高温分解;过滤;
(5) NaClO 2 在氯元素有 +3 价降低为 -1 价,则 1mol NaClO 2 转移电子 4mol ,消毒效率为 4/90.5 , 1mol Na 2 FeO 4 转移电子为 3mol ,消毒效率为 3/166 , 1molCl 2 转移电子为 2mol ,消毒效率为 2/71 ,三种消毒杀菌剂的消毒效率由大到小的顺序为: NaClO 2 >Cl 2 > Na 2 FeO 4 ,故答案为: NaClO 2 >Cl 2 > Na 2 FeO 4 ;