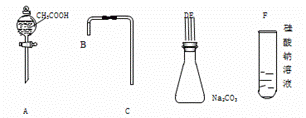
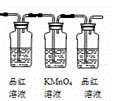
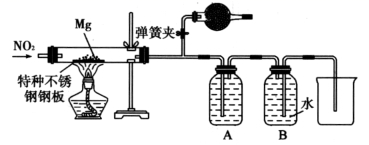
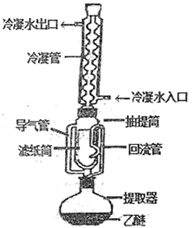
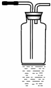如图是一 “ 套制取并验证氯气部分化学性质的实验装置。

回答下列问题:
(1) 装置 A 中,仪器 a 的名称为 __ ,写出 A 装置中发生反应的离子方程 __ 。
(2) 能证明氯的非金属性大于碘的实验现象是 __ 。
(3)D 的实验现象是 __ 。
(4) 通过查阅资料可知,二氧化锰和浓盐酸的反应可分步进行:
第一步: MnO 2 +2H 2 O=Mn(OH) 4 ( 快反应 )
第二步: __( 快反应 )
第三步: MnCl 4 =MnCl 2 +2Cl( 慢反应 )
第四步: Cl+Cl=Cl 2 ↑( 快反应 )
①请补充并写出第二步反应的化学方程式 ___ 。
②已知水溶液中 MnCl 4 为绿色, MnCl 2 为浅粉色,能证明发生了第三步反应的实验现象是 ___ 。
答案
分液漏斗 MnO 2 +4H + +2Cl - Mn 2+ +Cl 2 ↑+2H 2 O C 中溶液变蓝色 干燥布条缓慢褪色 Mn(OH) 4 +4HCl=MnCl 4 +4H 2 O 反应过程中,溶液出现绿色
【分析】
由实验装置可知, a 为分液漏斗, A 中发生 MnO 2 +4H + +2Cl - Mn 2+ +Cl 2 ↑+2H 2 O , B 中饱和食盐水可除去 HCl , C 中溶液变蓝, D 中干燥的有色布条褪色,因在进入 D 之前氯气未干燥, E 中 NaOH 溶液吸收尾气,以此来解答。
【详解】
(1) 根据仪器结构可知,仪器 a 的名称为分液漏斗,其中盛放的试剂为浓盐酸,装置 A 为 MnO 2 与浓盐酸在加热条件下制取 Cl 2 ,则反应的离子方程式为: MnO 2 +4H + +2Cl - Mn 2+ +Cl 2 ↑+2H 2 O 。
(2) Cl 2 通入碘化钾淀粉溶液中,可以发生反应 ,,碘单质可以使淀粉溶液变蓝,装置 C 中的溶液会变成蓝色,则能证明氯的非金属性大于碘的实验现象是 C 中溶液变蓝色。
(3) 由于 Cl 2 中混有水, Cl 2 与水反应生成次氯酸,次氯酸具有漂白性,可以使得装置 D 中干燥的有色布条缓慢褪色。
(4) ①由题意知,第二步反应中:有 Mn(OH) 4 消耗、有 MnCl 4 生成,则有盐酸参加该反应、且元素化合价不变,第二步反应的化学方程式为: Mn(OH) 4 +4HCl=MnCl 4 +4H 2 O 。 ②已知第三步为慢反应、水溶液中 MnCl 4 为绿色, MnCl 2 为浅粉色,则绿色的 MnCl 4 褪色很缓慢,浅粉色 MnCl 2 浓度增加也缓慢,因此可以说:能证明发生了第三步反应的实验现象是反应过程中,溶液出现绿色。