用下列装置制备并检验 Cl 2 的性质,下列说法正确的是 ( )
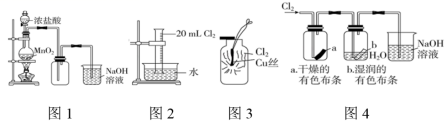
A . 图 1 :实验室制氯气,即使 MnO 2 过量,盐酸也不能全部反应完
B . 图 2 :充分光照后,溶液充满量筒
C . 图 3 :生成蓝色的烟,若在集气瓶中加入少量水,所得溶液呈绿色
D . 图 4 :干燥的有色布条不褪色,湿润的有色布条能褪色,说明 Cl 2 有漂白性
答案
A
【详解】
A .二氧化锰和浓盐酸在加热条件下发生氧化还原反应生成氯气,但稀盐酸与二氧化锰不反应,当盐酸浓度降低时,反应停止,则盐酸不能完全消耗,故 A 正确;
B . II 中涉及反应有 Cl 2 + H 2 O= HCl + HClO , 2HClO 2HCl +O 2 ↑,
,所以溶液达到量筒的一半,故 B 错误;
C .氯气与铜反应生成棕黄色的烟,加水溶液呈蓝色,故 C 错误;
D .润的有色布条能退色,是由于发生, Cl 2 + H 2 O= HCl + HClO, , HClO 具有漂白性,而干燥的氯气没有漂白性,故 D 错误;
故选 A 。







 ,HClO具有强氧化性,漂白剂不用氯水,而是用Cl2制成漂白粉的原因是便于贮存运输。
,HClO具有强氧化性,漂白剂不用氯水,而是用Cl2制成漂白粉的原因是便于贮存运输。