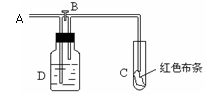
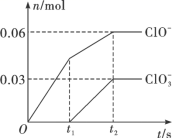
将一定量的 Cl 2 通入一定浓度的苛性钾溶液中,两者恰好完全反应 ( 已知反应过程放热 ) ,生成物中有三种含氯元素的离子,其中 ClO - 和 ClO 两种离子的物质的量 (n) 与反应时间 (t) 的变化示意图如图所示。下列说法不正确的是 ( )
A . 标况下,消耗 Cl 2 的体积为 2.016L
B . 反应中转移电子的物质的量是 0.21mol
C . 该反应的氧化产物有两种
D . 苛性钾溶液中 KOH 的质量是 16.8g
答案
A
【分析】
氯气和氢氧化钾溶液反应生成次氯酸钾、氯化钾和氯酸钾,根据图象知 n (ClO - )=0.06mol , n (ClO )=0.03mol ,根据电子转移守恒可知生成的氯离子 n (Cl - )=0.06mol×(1-0)+0.03mol×(5-0)=0.21mol ,故转移电子物质的量为 0.21mol ,根据电荷守恒可知 n (K + )= n (Cl - )+ n (ClO - )+ n (ClO
)=0.21mol+0.06mol+0.03mol=0.3mol ,结合 m = nM 计算氢氧化钾质量。
【详解】
A .根据分析可知 n (Cl - )+ n (ClO - )+ n (ClO )=0.3mol ,根据元素守恒可知 n (Cl 2 )=0.15mol ,标况下体积为 0.15mol × 22.4L/mol=3.36L , A 错误;
B .该反应中转移电子的物质的量 =0.06mol×(1-0)+0.03mol×(5-0)=0.21mol , B 正确;
C .氯气和氢氧化钾溶液反应的氧化产物有次氯酸钾和氯酸钾,共两种, C 正确;
D .通过以上分析知,氢氧化钾的物质的量 =0.3mol ,则氢氧化钾质量 =0.3mol×56g/mol=16.8g , D 正确;
综上所述答案为 A 。




 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。  2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。  HCl+HClO
HCl+HClO