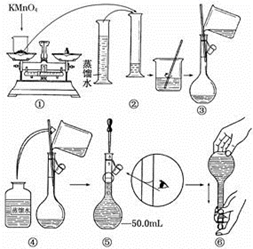
实验室需要 0.3 mol·L -1 NaOH 溶液 480mL 和一定浓度的硫酸溶液。根据这两种溶液的配制情况回答下列问题:
(1) 如图所示的仪器中配制溶液肯定不需要的是 _______ ( 填序号 ) ,配制上述溶液还需用到的玻璃仪器是 _______ ( 填仪器名称 ) 。

(2) 在配制 NaOH 溶液时:
①根据计算用托盘天平称取 NaOH 的质量为 _______ g ;
②若 NaOH 溶液在转移至容量瓶时,洒落了少许溶液,则所得溶液的浓度 _______ ( 填 “>” 、 “ < ” 或 “=”)0.3 mol·L -1 。
③下列主要操作步骤的正确顺序是 _______ ( 填序号 ) 。
A. 称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
B. 加水至液面离容量瓶瓶颈刻度线下 1 ~ 2 cm 时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
C. 待冷却至室温后,将溶液转移到 500mL 容量瓶中;
D. 盖好瓶塞,反复上下颠倒,摇匀;
E. 用少量蒸馏水洗涤烧杯内壁和玻璃棒 2 ~ 3 次,洗涤液转移到容量瓶中。
(3) 实验室采购了 98% (ρ=1.84g·cm -3 ) 的硫酸配制 3.68 mol·L -1 的硫酸溶液 250mL ,该同学实际配制硫酸溶液的浓度为 3.50 mol·L -1 ,原因可能是 _______ ( 填序号 ) 。
A. 用胶头滴管加水时俯视刻度
B. 容量瓶中原来存有少量水
C. 稀释硫酸的烧杯移液后未洗涤
D. 用胶头滴管加水定容时仰视刻度
(4) 若在滴加蒸馏水时,不慎超过了刻度线,此时的处理措施是 _______ 。
答案
AC 玻璃棒和烧杯 6.0 < ACEBD CD 重新配制
【分析】
用固体配制一定物质的量浓度溶液的一般步骤为计算、称量、溶解、冷却、转移、洗涤、定容、摇匀、装瓶贴签等,结合步骤分析解答。
【详解】
(1) 配制溶液肯定不需要的是分液漏斗和圆底烧瓶,配制上述溶液需用到的仪器有 500mL 容量瓶和烧杯,量筒,胶头滴管和玻璃棒等,图中还少的玻璃仪器为玻璃棒和烧杯;
(2) ①选取 500mL 容量瓶, NaOH 的质量为 m=0.3 mol·L -1 ×0.5L×40g/mol=6.0g ;
②若 NaOH 溶液在转移至容量瓶时,洒落了少许溶液,溶质有损失,则所得溶液的浓度 < 0.3mol/L ;
③配制溶液的步骤为计算,称量,溶解,冷却,转移,洗涤,定容,摇匀,装瓶贴签等,故顺序为: ACEBD ;
(3) A. 用胶头滴管加水时俯视刻度,溶液的体积变小,浓度偏大;
B. 容量瓶中原来存有少量水不影响最终浓度;
C. 稀释硫酸的烧杯移液后未洗涤,溶质有损失,浓度偏小;
D. 用胶头滴管加水定容时仰视刻度,溶液的体积变大,浓度偏小;
故选 CD ;
(4) 若在滴加蒸馏水时,不慎超过了刻度线,此时的处理措施是重新配制。