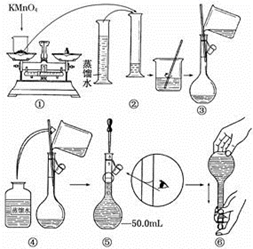
实验室用 NaOH 固体配制 250 mL1.25 mol/L 的 NaOH 溶液,请回答下列问题:
(1) 配制时必须的玻璃仪器有:烧杯、玻璃棒、胶头滴管、 _______ 。
(2) 用托盘天平称取 _______ g 固体 NaOH 。
(3) 配制时,其正确的操作顺序是 ( 字母表示,每个字母只能用一次 ) _______ ;
A .用 30 mL 水洗涤烧杯 2~3 次,洗涤液均注入容量瓶,振荡
B .用天平准确称取所需的 NaOH 的质量,加入少量水 ( 约 30 mL) ,用玻璃棒慢慢搅动,使其充分溶解
C .将已冷却的 NaOH 溶液沿玻璃棒注入 250mL 的容量瓶中
D .将容量瓶盖紧,颠倒摇匀
E .改用胶头滴管加水,使溶液凹面恰好与刻度相切
F .继续往容量瓶内小心加水,直到液面接近刻度 1~2cm 处
(4) 下列配制的溶液浓度偏低的是 _______ ;
A .向容量瓶中转移溶液时 ( 实验步骤 C) 不慎有液滴洒在容量瓶外面
B .加蒸馏水时不慎超过了刻度线
C .定容时俯视刻度线
D .配制前,容量瓶中有少量蒸馏水
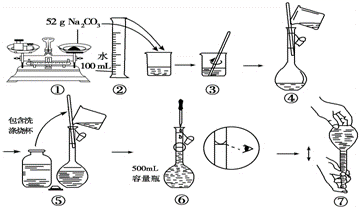
(5) 某同学改用固体 Na 2 CO 3 配制 Na 2 CO 3 溶液的过程如图所示,其错误 操作序号 是 _______ 。
(6) 如果固体 Na 2 CO 3 中混有少量杂质 Na 2 SO 4 ,可按规定程序检测出来。请写出所加的试剂和顺序 _______ 。
答案
250 mL 的容量瓶 12.5 BCAFED AB ①⑥ 先加稀盐酸,再加氯化钡溶液
【分析】
配制一定体积一定物质的量浓度的溶液需使用一定规格的容量瓶,根据 m = n ·M= c ·V·M 计算溶质的质量,结合配制溶液的步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶、贴签判断步骤先后顺序和使用的仪器;根据 c = 分析实验误差。
【详解】
(1) 根据配制溶液的步骤可知配制时必须的玻璃仪器有:烧杯、玻璃棒、胶头滴管、 250 mL 的容量瓶;
(2) 在实验室中有规格是 250 mL 的容量瓶,配制 250 mL1.25 mol/L 的 NaOH 溶液,需称量 NaOH 的质量 m (NaOH)=1.25 mol/L×0.25 L×40 g/mol=12.5 g ;
(3) 根据配制一定体积一定物质的量浓度溶液的步骤可知上述操作顺序为: BCAFED ;
(4) 根据配制溶液的浓度公式 c = 分析实验误差。
A .向容量瓶中转移溶液时 ( 实验步骤 C) 不慎有液滴洒在容量瓶外面,导致溶质损失,使配制的溶液浓度偏低, A 符合题意;
B .加蒸馏水时不慎超过了刻度线,溶液的体积偏大,由于溶质的物质的量不变,则配制的溶液浓度偏低, B 符合题意;
C .定容时俯视刻度线,会使溶液的体积偏小,由于溶质的物质的量不变,则导致配制的溶液浓度偏高, C 不符合题意;
D .配制前,容量瓶中有少量蒸馏水,不影响溶液的体积及溶质的物质的量,因此对配制溶液的浓度无影响, D 不符合题意;
故合理选项是 AB ;
(5) ① Na 2 CO 3 固体会腐蚀天平,应该在烧杯中进行称量,且天平使用应该是左物右码,图中药品和砝码位置也放反了, ①错误;
⑥用容量瓶配制溶液定容时,视线应该平视,不能仰视,⑥错误;其它各步操作均合理,故合理选项是①⑥;
(6) 如果固体 Na 2 CO 3 中混有少量杂质 Na 2 SO 4 ,检验的方法是向其中先加足量稀盐酸,使 Na 2 CO 3 转化为 CO 2 气体逸出,然后再加氯化钡溶液,若产生白色沉淀,就说明溶液中含有 Na 2 SO 4 ,发生反应: Na 2 SO 4 +BaCl 2 =BaSO 4 ↓+2NaCl 。