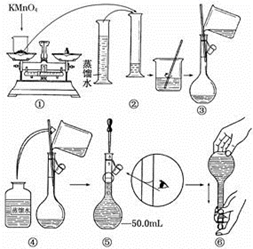
某学生欲配制 5.0mo1·L -1 的 H 2 SO 4 溶液 980mL ,实验室有两种不同体积、不同浓度的 H 2 SO 4 溶液:
① 200mL 质量分数为 49% 的 H 2 SO 4 溶液 ( 密度 ρ=1.40g·mL -1 ) ;
②足量的 18mo1·L 的 H 2 SO 4 溶液。
有三种规格的容量瓶: 250mL 、 500mL 、 1000mL 。
请回答下列问题:
(1) 质量分数为 49% 的 H 2 SO 4 溶液的物质的量浓度为 __ mo1·L -1 ? ( 结果保留一位小数 )
(2) 老师要求配制溶液时将 ①溶液全部用完后再用②溶液配制,则还需要②溶液 __ mL 。
(3) 配制该 H 2 SO 4 溶液应选用容量瓶的规格为 __ mL 。
(4) 配制时,该同学的操作顺序如下,请将操作步骤 D 补充完整。
A. 将 ①溶液全部倒入烧杯中;
B. 用量筒准确量取所需的 18mo1·L 的 H 2 SO 4 溶液,沿烧杯内壁倒入上述溶液中,并用玻璃棒搅拌,使其混合均匀;
C. 将混合均匀的 H 2 SO 4 溶液沿玻璃棒注入所选的容量瓶中;
D. 用适量的蒸馏水 __ ,然后 __ 容量瓶中;
E. 振荡,继续向容量瓶中加水,直到液面接近刻度线 1-2cm 处;
F. 改用 __ 加水,使 __ 与刻度线相切;
G. 将容量瓶盖紧,摇匀。
(5) 以下操作会造成所配溶液浓度偏小的有 __ 。 ( 填字母符号 )
A. 仰视量筒刻度线;
B. 省略 (4) 中操作 D ;
C. 转移时少量液体流出;
D. 不冷却至室温就将烧杯中的溶液转移入容量瓶中;
E. 仰视容量瓶刻度线
答案
7.0 200 1000 洗涤烧杯和玻璃棒 2-3 次 将洗液转移到 胶头滴管 液面最凹处 B 、 C 、 E
【分析】
( 5 )分析操作对溶质物质的量和溶液体积的影响,依据 进行误差分析。
【详解】
( 1 )质量分数为 49% 的 H 2 SO 4 溶液的物质的量浓度为 ,
故答案为: 7.0 ;
( 2 )配制 5.0mol • L -1 的 H 2 SO 4 溶液 980mL ,应选择 1000mL 容量瓶,设需要 ②溶液体积为 V ,则依据溶液稀释过程中溶质物质的量不变得 7.0mol/L × 200mL+18mol/L × V =5.0mol • L -1 × 1000mL ,解得 V =200.0mL ,故答案为: 200.0 ;
( 3) 配制 5.0mol • L -1 的 H 2 SO 4 溶液 980mL ,应选择 1000mL 容量瓶,故答案为: 1000 ;
( 4 ) D 洗涤正确操作为:用适量的蒸馏水 洗涤烧杯和玻璃棒 2-3 次,然后将洗涤液全部转移到容量瓶中, F 定容的操作为:改用胶头滴管逐滴滴加到凹液面最低处与刻度线相切,故答案为:洗涤烧杯和玻璃棒 2-3 次;将洗涤液全部转移到;胶头滴管;凹液面最最低处;
( 5 ) A .仰视量筒刻度线,导致量取浓溶液体积偏大,溶质物质的量偏大,溶液浓度偏高,故不选;
B .省略 (4)中操作 D ,导致溶质物质的量偏小,溶液浓度偏低,故选;
C .转移时少量液体流出,导致溶质物质的量偏小,溶液浓度偏低,故选;
D .不冷却至室温就将烧杯中的溶液转移入容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故不选;
E .仰视容量瓶刻度线,导致溶液体积偏大,溶液浓度偏低,故选,故答案为: BCE 。