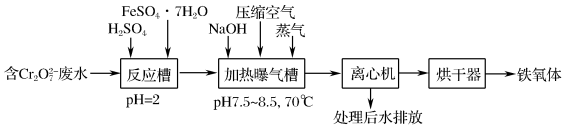
Cr( Ⅵ ) 对 A 体具有致癌、致突变作用。铁氧体法 ( 铁氧体是组成类似于 Fe 3 O 4 的复合氧化物,其中部分 Fe( Ⅲ ) 可被 Cr( Ⅲ ) 等所代换 ) 是目前处理 Cr( Ⅵ ) 废水的常见方法之一,其工艺流程如下:
(1)Cr( Ⅵ ) 包括 CrO 和 Cr 2 O
,我国排放标准是每升废水铬元素含量不超过 0.5 mg·L -1 。
①转化反应: 2CrO +2H + ⇌ Cr 2 O
+H 2 O 的平衡常数表达式 K= ______ 。
②取某 Cr( Ⅵ ) 废水 ( 只含 CrO ) 与 2.0×1 0 -4 mol·L -1 AgNO 3 溶液等体积混合,有棕红色 Ag 2 CrO 4 沉淀,则原废水中六价铬超标 ______ 倍以上
![]() 。
。
(2) 铁氧体法处理含 Cr 2 O 废水的工艺流程中:
① “ 反应槽 ” 中发生反应的离子方程式为 ______ 。
②在 “ 加热曝气槽 ” 中通入压缩空气的目的是 ______ 。
答案
20.8 Cr 2 O
+6Fe 2+ +14H + =2Cr 3+ +6Fe 3+ +7H 2 O 将部分 Fe(OH) 2 氧化为 Fe(OH) 3 以形成铁氧体
【分析】
含 Cr 2 O 的废水加入稀硫酸调节 pH=2,加入硫酸亚铁发生氧化还原反应生成铁离子,加入氢氧化钠并调节pH可生成铁氧体,离心分离,烘干得到产物,据此回答。
【详解】
(1) ①平衡常数中不写入固体和纯液体, 2CrO +2H + ⇌ Cr 2 O
+H 2 O 的平衡常数表达式 K=
。
②设废水中 CrO ![]() 的浓度为 x mol·L -1 ,与 AgNO 3 溶液等体积混合后, CrO
的浓度为 x mol·L -1 ,与 AgNO 3 溶液等体积混合后, CrO ![]() 的浓度变成
的浓度变成 mol·L -1 , c(AgNO 3 )=
mol·L -1 =1.0×10 -4 mol·L -1 , K sp (Ag 2 CrO 4 )=c 2 (Ag + )·c(CrO
![]() )=(1.0×10 -4 ) 2 ×
)=(1.0×10 -4 ) 2 × =1.0×10 -12 ,得 x=2.0×10 -4 mol·L -1 , Cr 含量: (2.0×10 -4 mol ×52 g·mol -1 ×1 000 mg/g)/L=10.4 mg·L -1 ,超标为:
=20.8 倍。
(2) ①反应槽中, Cr 2 O ![]() 在酸性条件下氧化 Fe 2+ ,生成 Fe 3+ 和 Cr 3+ ,根据 Fe 和 Cr 得失电子守恒,用 H + 平衡电荷,则离子方程式为 Cr 2 O
在酸性条件下氧化 Fe 2+ ,生成 Fe 3+ 和 Cr 3+ ,根据 Fe 和 Cr 得失电子守恒,用 H + 平衡电荷,则离子方程式为 Cr 2 O +6Fe 2+ +14H + =2Cr 3+ +6Fe 3+ +7H 2 O 。
②反应槽中 Fe 2+ 是过量的,在 “ 加热曝气槽 ” 中,加入 NaOH 会生成 Fe(OH) 2 ,压入空气,可以将 Fe(OH) 2 氧化为 Fe(OH) 3 ,最终可以转化铁氧体中的 Fe 3+ 。
