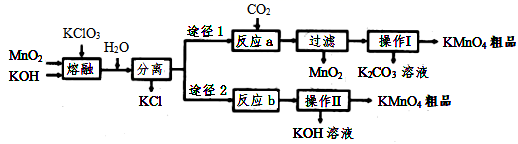
高锰酸钾是中学化学常用的试剂。主要用于防腐、化工、制药等。实验室模拟工业上用软锰矿制备高锰酸钾的流程如下:
(1) 实验室熔融二氧化锰、氧氧化钾、氯酸钾时应选择哪一种仪器 _______
a. 普通玻璃坩埚 b. 石英坩埚 c. 陶瓷坩埚 d. 铁坩埚
(2) 第一步熔融时生成 K 2 MnO 4 的化学方程式: _______
(3) 操作 Ⅰ中根据 KMnO 4 和 K 2 CO 3 两物质在 _______ ( 填性质 ) 上的差异,采用浓缩结晶、趁热过滤得到 KMnO 4 。趁热过滤的原因是 _______
(4)KMnO 4 常用在实验室制取氧气,其产物常做电池材料,其中碱性电池锌 — 锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO 2 (s)+H 2 O(l)=Zn(OH) 2 (s)+Mn 2 O 3 (s) 。电池工作时,锌做 _______ 极,电池正极的电极反应式为 _______ 外电路中每通过 0.2mol 电子,锌的质量理论上减小 _______ g
(5)KMnO 4 稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的 _______ ( 填标号 )
a. 双氧水 b.84 消液 (NaClO 溶液 ) c.75 %酒精
答案
d 3MnO 2 +KClO 3 +6KOH 3K 2 MnO 4 +KCl+3H 2 O 溶解性 避免温度下降,造成主产品的纯度降低 负 2MnO 2 +H 2 O+2e - =Mn 2 O 3 +2OH - 6.5g ab
【分析】
根据题中流程图可知,二氧化锰、氢氧化钾、氯酸钾熔融发生反应: 3MnO 2 +KClO 3 +6KOH 3K 2 MnO 4 +KCl+3H 2 O ;加水溶解,分离出 KCl ,得到 K 2 MnO 4 溶液;向 K 2 MnO 4 溶液中通入二氧化碳得到 KMnO 4 、 MnO 2 、 K 2 CO 3 ,过滤除去滤渣 MnO 2 ,滤液为 KMnO 4 、 K 2 CO 3 溶液,浓缩结晶,趁热过滤得到 KMnO 4 晶体,滤液中含有 K 2 CO 3 。
【详解】
(1) 实验室熔融二氧化锰、氧氧化钾、氯酸钾时应选择铁坩埚,因为普通玻璃坩埚、石英坩埚、陶瓷坩埚中的二氧化硅均与 KOH 反应,故答案为: d ;
(2) 第一步熔融时二氧化锰、氧氧化钾、氯酸钾发生反应生成 K 2 MnO 4 的化学方程式为: 3MnO 2 +KClO 3 +6KOH 3K 2 MnO 4 +KCl+3H 2 O ;
(3) 采用浓缩结晶、趁热过滤得到 KMnO 4 ,说明高锰酸钾的溶解性随温度变化较大,操作 Ⅰ 中根据 KMnO 4 和 K 2 CO 3 两物质在溶解性上的差异,采用浓缩结晶、趁热过滤得到 KMnO 4 ,趁热过滤的原因是避免温度下降,造成主产品纯度降低,故答案为:溶解性;避免温度下降,造成主产品纯度降低;
(4) 电池工作时 Zn 失电子,故 Zn 为负极;电池正极的电极反应式为 2MnO 2 +H 2 O+2e - =Mn 2 O 3 +2OH - ; Zn+2OH - -2e - = Zn(OH) 2 ,外电路中每通过 0.2mol 电子,锌的质量理论上减小 ;
(5) KMnO 4 稀溶液因为其强氧化性是一种常用的消毒剂,双氧水、 84 消液 (NaClO 溶液 ) 具有强氧化性能消毒,酒精消毒是因为其能使组成细菌的蛋白质变性,故答案为: ab 。
