按要求完成下列填空:
(1) 硫酸钡的电离方程式: _______ 。
(2) 盐酸和小苏打反应离子方程式: _______ 。
(3) 向硫酸氢钠溶液中逐滴加入氢氧化钡,溶液恰好显中性时反应的离子方程式: _______ 。
(4) 向澄清石灰水中通入过量 CO 2 反应的离子方程式: _______ 。
(5) 配平下列方程式,并用双线桥表示电子转移的数目与氧化还原、化合价变化之间的关系: +Fe 2+ +____=Mn 2+ +Fe 3+ +____ , ___________ 。
答案
BaSO 4 =Ba 2+ +
+H + =CO 2 ↑+H 2 O Ba 2+ +2OH ﹣ +
+2H + =BaSO 4 ↓+2H 2 O OH ﹣ +CO 2 =
【详解】
(1) 硫酸钡为强电解质,在水溶液中完全电离,其电离方程式为 BaSO 4 =Ba 2+ + ;故答案为 BaSO 4 =Ba 2+ +
;
(2) 小苏打为 NaHCO 3 ,与盐酸反应的离子方程式为 +H + =CO 2 ↑+H 2 O ;故答案为
+H + =CO 2 ↑+H 2 O ;
(3) 两种溶液反应后显中性, 1molBa(OH) 2 消耗 2molNaHSO 4 ,即离子方程式为 Ba 2+ +2OH ﹣ + +2H + =BaSO 4 ↓+2H 2 O ;故答案为 Ba 2+ +2OH ﹣ +
+2H + =BaSO 4 ↓+2H 2 O ;
(4)CaCO 3 能与 CO 2 反应生成 Ca(HCO 3 ) 2 ,即澄清石灰水中通入足量的 CO 2 ,发生的离子方程式为 OH ﹣ +CO 2 = ;故答案为 OH ﹣ +CO 2 =
;
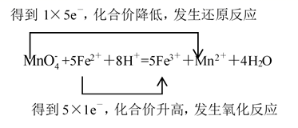
(5) 中 Mn 元素的化合价由+ 7 价 →+ 2 价,降低 5 价,铁元素的化合价由+ 2 价 →+ 3 价,化合价升高 1 价,最小公倍数为 5 ,即 Fe 2 + 前系数为 5 ,根据离子共存,该溶液显酸性,根据离子守恒,得出
+5Fe 2 + + 8H + =5Fe 3 + + Mn 2 + + 4H 2 O ,双线桥表示:
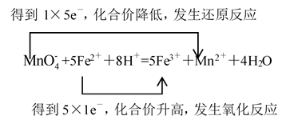 ,故答案为
,故答案为 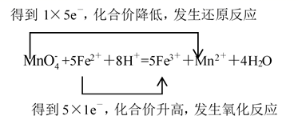 ;
;



