已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下: 3Cu+8HNO 3 ( 稀 )=3Cu(NO 3 ) 2 +2NO↑+4H 2 O 。
(1) 用双线桥 ( 或单线桥 ) 标出电子转移的方向和数目 ______ 。
(2) 被氧化的元素是 ____ ,发生氧化反应的物质是 ____ ,还原产物是 _____ 。
答案
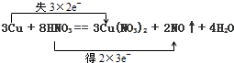 或
或 ![]() Cu Cu NO
Cu Cu NO
【分析】
3Cu+8HNO 3 ═3Cu ( NO 3 ) 2 +2NO↑+4H 2 O 中, Cu 元素的化合价由 0 升高为 +2 价, N 元素的化合价由 +5 价降低为 +2 价,以此来解答。
【详解】
(1)3Cu+8HNO 3 ═3Cu(NO 3 ) 2 +2NO↑+4H 2 O 中, Cu 元素的化合价由 0 升高为 +2 价, N 元素的化合价由 +5 价降低为 +2 价,该反应中转移 6e − ,电子得失的方向和数目为  或
或 ![]() 。
。
(2)N 元素的化合价降低,则 HNO 3 为氧化剂,生成还原产物 NO , Cu 元素失去电子被氧化,发生氧化反应,则 Cu(NO 3 ) 2 或 Cu 2+ 为氧化产物,故答案为: Cu ; Cu ; NO 。
