用软锰矿 ( 主要成分为 MnO 2 ,含少量 Fe 3 O 4 、 Al 2 O 3 ) 和 BaS 制备高纯 MnCO 3 的工艺流程如下:
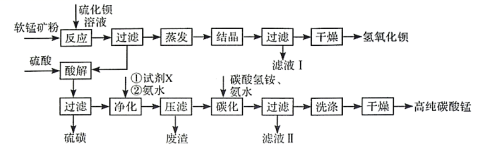
软锰矿预先粉碎的目的是 ____________ , MnO 2 与 BaS 溶液反应转化为 MnO 的化学方程式为 ________ 。
答案
增大接触面积,充分反应,提高反应速率 MnO 2 +BaS+H 2 O=Ba(OH) 2 +MnO+S
【详解】
软锰矿预先粉碎可以增大反应物的接触面积,使反应更充分,提高反应速率; MnO 2 与 BaS 反应转化为 MnO , Mn 元素的化合价由 +4 价降低为 +2 价,根据元素价态规律可知 -2 价的 S 元素应被氧化得到 S 单质,则 MnO 2 与 BaS 的系数比应为 1:1 ,根据后续流程可知产物还有 Ba(OH) 2 ,结合元素守恒可得化学方程式为: MnO 2 +BaS+H 2 O=Ba(OH) 2 +MnO+S 。



