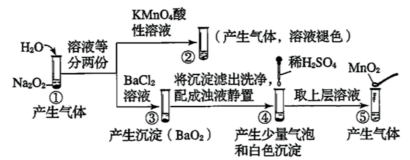
探究 Na 2 O 2 与水的反应,实验如图:
已知: H 2 O 2 ⇌ H + +HO 、 HO
⇌ H + +O
下列分析不正确的是
A . ①、⑤中产生的气体能使带火星的木条复燃
B . ①、④中均发生了氧化还原反应和复分解反应
C . ②、⑤中 KMnO 4 与 MnO 2 的作用不同,产生气体的量也不同
D . 沉淀经过滤、洗涤、干燥后称量: ④中反应后的沉淀质量小于③中所得沉淀的质量
答案
D
【分析】
过氧化钠和水反应生成气体为氧气,反应后的溶液加入高锰酸钾酸性溶液,生成气体,且高锰酸钾溶液褪色,说明过氧化钠与水反应生成过氧化氢,可被高锰酸钾氧化生成氧气;加入氯化钡生成 BaO 2 沉淀,浊液中加入稀硫酸生成硫酸钡沉淀和 H 2 O 2 ,加入二氧化锰催化双氧水分解生成氧气,以此解答该题。
【详解】
A .根据分析 ①、⑤中产生的气体为氧气,能使带火星的木条复燃,故 A 正确;
B . ①中产生气体,说明过氧化钠和水发生了氧化还原反应,根据后续实验可知①中同时发生反应: 2H 2 O+Na 2 O 2 =H 2 O 2 +2NaOH ,该反应属于复分解反应; ④中 BaO 2 与 H 2 SO 4 发生反应: BaO 2 +H 2 SO 4 =BaSO 4 +H 2 O 2 ,该反应属于氧化还原反应,产生少量气泡,说明双氧水分解产生氧气,该反应为氧化还原反应,故 B 正确;
C . ②中高锰酸钾将 H 2 O 2 氧化,为氧化剂, -1 价的 O 全部转化为 O 2 ; ⑤中 MnO 2 为 H 2 O 2 分解的催化剂, -1 价的 O 只有一半转化为 O 2 ,所以 ②、⑤中 KMnO 4 与 MnO 2 的作用不同,产生气体的量也不同,故 C 正确;
D . ③中沉淀为 BaO 2 , ④中 BaO 2 全部转化为 BaSO 4 沉淀,根据 BaO 2 和 BaSO 4 的摩尔质量大小关系可知 ④中反应后的沉淀质量大于③中所得沉淀的质量,故 D 错误;
综上所述答案为 D 。

 B
B
 D
D