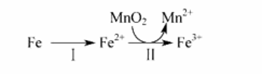“循环经济”和“低碳经济”是目前备受关注的课题,因而对碳、硫及其化合物的综合利用成为研究的热点。
( 1 )下列事实中,能用来比较碳元素和硫元素的非金属性强弱的是 ____________ (填字母)。
A . SO 2 具有漂白性而 CO 2 没有
B .少量 H 2 SO 3 可与 Na 2 CO 3 反应生成 NaHCO 3
C . SO 2 能使酸性 KMnO 4 溶液褪色而 CO 2 不能
D . Na 2 CO 3 溶液显碱性,而 Na 2 SO 4 溶液显中性
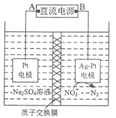
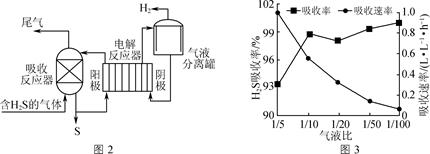
( 2 )通过热循环进行能源综合利用的反应系统的原理如下图所示。

系统( Ⅱ )制取氢气的热化学方程式为 ________________________ ;
两个系统制得等量的 H 2 时所需能量较少的是 ________________________ 。
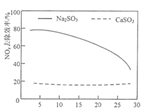
( 3 )向 10L 恒容密闭容器中充入 2 molCO 和 1molSO 2 ,发生反应 2CO ( g ) +SO 2 ( g ) ![]() S ( g ) +2CO 2 ( g )。 CO 和 CO 2 的平衡体积分数(
S ( g ) +2CO 2 ( g )。 CO 和 CO 2 的平衡体积分数( )与温度( T )的变化关系如下图所示。
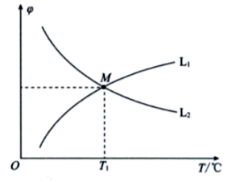
① 图中表示 CO 的平衡体积分数与温度的变化关系的曲线为 _____________ (填 “L 1 ” 或 “L 2 ” )。
②T 1 ℃ 时, SO 2 的平衡转化率 a 1 = _____________ ,反应的平衡常数 K 1 = _____________ 。
③ 只改变下列条件,既能加快该反应的反应速率,又能增大 CO 的平衡转化率的是 _____________ (填字母)。
A .增大压强
B .充入一定量的 H 2 S
C .充入一定量的 SO 2
D .加入适当催化剂
④ 向起始温度为 T 1 ℃ 的 10L 绝热容器中充入 2molCO 和 1molSO 2 ,重复实验,该反应的平衡常数 K 2 ___ (填 “ > ”“ < ” 或 “=” ) K 1 ,理由为 ______________________ 。
答案
D S ( g ) +2H 2 O ( g ) ![]() SO 2 ( g ) +2H 2 ( g ) △ H=-90.0kJ•mol -1 系统( Ⅱ) L 2 50% 1 C < 该反应为吸热反应,平衡时绝热容器内的温度低于恒温容器内的温度,平衡逆向移动,平衡常数减小
SO 2 ( g ) +2H 2 ( g ) △ H=-90.0kJ•mol -1 系统( Ⅱ) L 2 50% 1 C < 该反应为吸热反应,平衡时绝热容器内的温度低于恒温容器内的温度,平衡逆向移动,平衡常数减小
【分析】
(1) 比较非金属性,可利用非金属元素气态氢化物的稳定性,和最高价氧化物对应的水化物的酸性, S 的最高价的氧化物的水化物为硫酸,不能利用亚硫酸。
( 2 )盖斯定律求反应热。
【详解】
( 1 ) SO 2 具有漂白性,其原因为 SO 2 与有色物质反应生成不稳定的无色物质,与元素的非金属性无关, A 错误;少量 H 2 SO 3 可与 Na 2 CO 3 反应生成 NaHCO 3 ,证明 H 2 SO 3 的酸性强于 HCO 3 - 的酸性,但不能比较碳元素与硫元素的非金属性强弱, B 错误; SO 2 能使酸性 KMnO 4 溶液褪色 . 体现其还原性,低价态氧化物的还原性强弱不能用来比较元素的非金属性强弱, C 错误; Na 2 CO 3 溶液显碱性说明 H 2 CO 3 为弱酸, Na 2 SO 4 溶液显中性说明 H 2 SO 4 为强酸,最高价氧化物对应的水化物的酸性越强,元素的非金属性越强, D正确。答案选D;
( 2 )由信息知, ① CO 2 ( g ) +C ( s ) ![]() 2CO ( g ) △ H 1 = + 172.4 kJ • mol -1 , ② Fe 3 O 4 ( s ) +CO ( g )
2CO ( g ) △ H 1 = + 172.4 kJ • mol -1 , ② Fe 3 O 4 ( s ) +CO ( g ) ![]() 3FeO ( s ) + CO 2 ( g ) △ H 2 =+ 17.2 kJ• mol -1 , ③ 3FeO ( s ) + H 2 O ( g )
3FeO ( s ) + CO 2 ( g ) △ H 2 =+ 17.2 kJ• mol -1 , ③ 3FeO ( s ) + H 2 O ( g ) Fe 3 O 4 ( s ) + H 2 ( g ) △ H 3 = -58. 2 kJ·mol -1 , ④ 2CO ( g ) +SO 2 ( g )
S ( g ) +2CO 2 ( g ) △ H 4 = +8.0 kJ• mol -1 ,应用盖斯定律得系统( Ⅰ)中热化学碳水循环制取氢气的热化学方程式为① + ② ×2+ ③ ×2 ,即 C ( s ) + 2H 2 O ( g )
![]() CO 2 ( g ) +2H 2 ( g ) △ H=+90.4 kJ• mol -1 ;系统( Ⅱ)中热化学硫水循环联产氢气和二氧化硫的热化学方程式为② ×2 + ③ ×2 - ④,即 S ( g ) +2H 2 O ( g )
CO 2 ( g ) +2H 2 ( g ) △ H=+90.4 kJ• mol -1 ;系统( Ⅱ)中热化学硫水循环联产氢气和二氧化硫的热化学方程式为② ×2 + ③ ×2 - ④,即 S ( g ) +2H 2 O ( g ) ![]() SO 2 ( g ) +2H 2 ( g ) △ H= -90.0 kJ• mol -1 。系统( Ⅰ)为吸热反应,系统(Ⅱ)为放热反应,故制得等量的 H 2 时所需能量较少的是系统( Ⅱ)。答案为 S ( g ) +2H 2 O ( g )
SO 2 ( g ) +2H 2 ( g ) △ H= -90.0 kJ• mol -1 。系统( Ⅰ)为吸热反应,系统(Ⅱ)为放热反应,故制得等量的 H 2 时所需能量较少的是系统( Ⅱ)。答案为 S ( g ) +2H 2 O ( g ) ![]() SO 2 ( g ) +2H 2 ( g ) △ H= -90.0 kJ• mol -1 系统( Ⅱ);
SO 2 ( g ) +2H 2 ( g ) △ H= -90.0 kJ• mol -1 系统( Ⅱ);
( 3 ) ①该反应为吸热反应,温度升高,平衡正向移动, CO 的平衡体积分数减小, CO 2 的平衡体积分数增大,故图中表示 CO 的平衡体积分数与温度的变化关系的曲线为 L 2 。答案为 L 2 ;
②由图中信息, T 1 ℃时, M 点对应体系中 CO 和 CO 2 的平衡体积分数相等,则平衡时 CO 和 CO 2 的物质的量相等,设参与反应的 SO 2 的物质的量为 x ,根据 “ 三段式 ” 法可得 2mol-2x=2x ,解得 x=0.5 mol ,故 SO 2 的平衡转化率 α 1 = ×100%=50% 。同时计算得 CO ( g )、 SO 2 ( g )、 S ( g )、 CO 2 ( g )的平衡浓度分别为 0.1 mol•L -1 、 0.05mol•L -1 、 0. 05 mol•L -1 、 0.1mol•L -1 ,故该反应的平衡常数 K 1 =1 。答案为 50% 1 ;
③该反应为反应前后气体分子数不变的吸热反应,故增大压强,平衡不移动, A 错误;充入一定量 H 2 S 后,其与 SO 2 反应生成硫单质,平衡逆向移动, CO 的平衡转化率减小,反应速率减小, B 错误;充入一定量 SO 2 , SO 2 的浓度增大,平衡正向移动, CO 的平衡转化率增大,反应速率加快, C 正确;加入催化剂,平衡不移动, D 错误。答案选 C;
④该反应为吸热反应,平衡时绝热容器内的温度低于恒温容器内的温度,平衡逆向移动,平衡常数减小。答案为 < 该反应为吸热反应,平衡时绝热容器内的温度低于恒温容器内的温度,平衡逆向移动,平衡常数减小。