氮氧化合物是目前造成大气污染的主要气体,而汽车尾气中就含有 NO 等多种污染气体。汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致。请结合所学知识回答下列问题:
(1) 已知:N 2 (g)+2O 2 (g) ![]() 2NO 2 (g) △H 1 =+67.8 kJ/mol
2NO 2 (g) △H 1 =+67.8 kJ/mol
2NO 2 (g) ![]() O 2 (g)+2NO(g) △H 2 =+116.2 kJ/mol
O 2 (g)+2NO(g) △H 2 =+116.2 kJ/mol
则 N 2 (g)+O 2 (g) ![]() 2NO(g) △H= _________ kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为 _____________
2NO(g) △H= _________ kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为 _____________
(2) 若反应N 2 (g)+O 2 (g) ![]() 2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是 ________
2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是 ________
a.2υ 正 (N 2 )= υ 逆 (NO) b.混合气体密度不变
c.生成1molO 2 的同时生成 2molNO d.混合气体平均相对分子质量不变
(3) 汽车尾气净化反应:2NO(g)+2CO(g) ![]() N 2 (g)+2CO 2 (g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
N 2 (g)+2CO 2 (g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
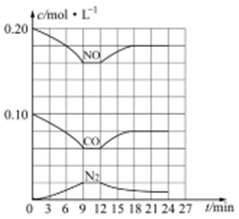
①该反应能自发进行的条件为 _____ (填“高温”、“低温”或“任意温度”);
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)= ________ mol·L -l ·min -1 ;
③第12min时改变的反应条件为 _________ (填“升高温度”或“降低温度”);
④反应在第24min时的平衡常数K= ____________ (只列出计算式,无需计算结果),若保持温度不变,再向容器中充入CO、N 2 各 0.060mol,平衡将 _________ 移动 (填“正向”、“逆向”或“不”)。
答案
+184.0 温度升高,反应速率加快;且温度升高有利于平衡正向移动 ac 低温 0.0067 升高温度 ![]() 逆向
逆向
【解析】
试题分析:本题考查盖斯定律的应用、化学平衡的标志、化学平衡图像的分析、外界条件对化学反应速率和化学平衡的影响、化学反应速率和化学平衡常数的计算 、 化学反应自发性的判断 。
( 1 )对反应编号, N 2 ( g)+2O 2 ( g) ![]() 2NO 2 ( g) △H 1 =+67.8 kJ/mol(① 式)
2NO 2 ( g) △H 1 =+67.8 kJ/mol(① 式)
2NO 2 ( g) ![]() O 2 ( g)+2NO(g) △H 2 =+116.2 kJ/mol(② 式)
O 2 ( g)+2NO(g) △H 2 =+116.2 kJ/mol(② 式)
应用盖斯定律,将 ① 式 +② 式得, N 2 ( g)+O 2 ( g) ![]() 2NO(g) △H=ΔH 1 +ΔH 2 =(+67.8kJ/mol)+(+116.2kJ/mol)=+184.0kJ/mol。 汽车启动后,气缸温度越高,单位时间内 NO 的排放量越大,其原因是 : 温度升高,反应速率加快;且温度升高有利于平衡正向移动。
2NO(g) △H=ΔH 1 +ΔH 2 =(+67.8kJ/mol)+(+116.2kJ/mol)=+184.0kJ/mol。 汽车启动后,气缸温度越高,单位时间内 NO 的排放量越大,其原因是 : 温度升高,反应速率加快;且温度升高有利于平衡正向移动。
( 2)a 项 , 2υ 正 ( N 2 ) =υ 逆 ( NO )表示正、逆反应速率相等,能说明反应已达到平衡状态; b 项 , 根据质量守恒定律,混合气体的总质量始终不变,在恒容容器中,混合气体的密度始终不变,混合气体的密度不变不能说明反应已达到平衡状态; c 项 , 生成 1molO 2 一定消耗 2molNO ,生成 1molO 2 的同时生成 2molNO ,说明各物质的浓度保持不变,能说明反应已达到平衡状态; d 项 , 根据质量守恒定律,混合气体的总质量始终不变,该反应反应前后气体分子数不变,建立平衡过程中气体分子总物质的量始终不变,混合气体平均相对分子质量始终不变,混合气体平均相对分子质量不变不能说明反应已达到平衡状态;能说明反应已达到平衡状态的是 ac, 答案选 ac。
( 3)① 反应 2NO(g)+2CO(g) ![]() N 2 ( g)+2CO 2 ( g) 的 Δ H=-746.5kJ/mol
N 2 ( g)+2CO 2 ( g) 的 Δ H=-746.5kJ/mol ![]() 0、ΔS
0、ΔS ![]() 0 ,该反应能自发进行时 ΔG=ΔH-TΔS
0 ,该反应能自发进行时 ΔG=ΔH-TΔS ![]() 0 ,可见该反应自发进行的条件为低温。
0 ,可见该反应自发进行的条件为低温。
② 根据图像 6~9min 内 , υ(CO)= ![]() =0.0067mol/(L·min)。
=0.0067mol/(L·min)。
③ 根据图像 , 第 12min 时改变条件,达到新平衡时 N 2 浓度减小, NO、CO 的浓度增大,改变条件平衡向逆反应方向移动,由于该反应的正反应为放热反应,所以改变的条件为升高温度。
④ 根据图像,结合三段式
2NO(g)+2CO(g) ![]() N 2 ( g)+2CO 2 ( g)
N 2 ( g)+2CO 2 ( g)
c (起始)( mol/L) 0.2 0.1 0 0
c (转化)( mol/L) 0.02 0.02 0.01 0.02
c(24min)(mol/L) 0.18 0.08 0.01 0.02
24min 时反应达到平衡状态,反应的平衡常数 K= ![]() =
= ![]() =0.01929 。若保持温度不变,再向容器中充入 CO、N 2 各 0.060mol, 此时 NO、CO、N 2 、 CO 2 物质的量浓度依次为 0.18mol/L、0.14mol/L、0.07mol/L、0.02mol/L, 此时的浓度商 Q c =
=0.01929 。若保持温度不变,再向容器中充入 CO、N 2 各 0.060mol, 此时 NO、CO、N 2 、 CO 2 物质的量浓度依次为 0.18mol/L、0.14mol/L、0.07mol/L、0.02mol/L, 此时的浓度商 Q c = ![]() =0.044
=0.044 ![]() 0.01929 ,平衡将逆向移动。
0.01929 ,平衡将逆向移动。
