依据事实,书写下列热化学方程式:
( 1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH 2 ,吸热 131.5kJ: ______________________________________ 。
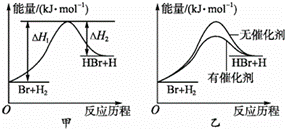
( 2)根据下图写出热化学方程式 __________________________________________ 。

( 3)已知稀溶液中,1 mol H 2 SO 4 与 NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H 2 SO 4 与 NaOH反应中和热的热化学方程式 __________________ 。
( 4)已知:2SO 2 (g)+O 2 (g) ![]() 2SO 3 (g) ΔH=-196.6 kJ·mol –1
2SO 3 (g) ΔH=-196.6 kJ·mol –1
2NO(g)+O 2 (g) ![]() 2NO 2 (g) ΔH=-113.0 kJ·mol –1
2NO 2 (g) ΔH=-113.0 kJ·mol –1
请写出 NO 2 与 SO 2 反应生成 SO 3 和 NO的热化学方程式 ____________________ 。
答案
C ( s )+ H 2 O ( g )= CO ( g )+ H 2 ( g ) △ H = + 131 . 5kJ / molN 2 ( g )+ 3H 2 ( g )= 2NH 3 ( g ) △ H =- 92kJ / mol1 / 2H 2 SO 4 ( aq )+ NaOH ( aq )= 1 / 2Na 2 SO 4 ( aq )+ H 2 O ( l ) △ H =- 57 . 3kJ / molNO 2 ( g )+ SO 2 ( g )= SO 3 ( g )+ NO ( g ) △ H =- 41 . 8kJ / mol
【解析】
( 1 )在 25 ℃、 101kPa 时, 1molC 与 1mol 水蒸气反应生成 1molCO 和 1molH 2 ,吸热 131 . 5kJ ,则反应的热化学方程式为 C ( s )+ H 2 O ( g )= CO ( g )+ H 2 ( g ) △ H = + 131 . 5kJ / mol 。
( 2 )根据图像可知反应物总能量高于生成物总能量,反应热是 508kJ / mol - 600kJ / mol =- 92kJ / mol ,所以热化学方程式为 N 2 ( g )+ 3H 2 ( g )= 2NH 3 ( g ) △ H =- 92kJ / mol 。
( 3 )已知稀溶液中, 1 mol H 2 SO 4 与 NaOH 溶液恰好完全反应时,放出 114 . 6 kJ 热量,由于中和热是在一定条件下,稀溶液中,强酸和强碱反应生成 1mol 水时所放出的热量,所以表示 H 2 SO 4 与 NaOH 反应中和热的热化学方程式为 1 / 2H 2 SO 4 ( aq )+ NaOH ( aq )= 1 / 2Na 2 SO 4 ( aq )+ H 2 O ( l ) △ H =- 57 . 3kJ / mol 。
( 4 )已知:
① 2SO 2 ( g )+ O 2 ( g ) ![]() 2SO 3 ( g ) ΔH =- 196 . 6 kJ · mol – 1
2SO 3 ( g ) ΔH =- 196 . 6 kJ · mol – 1
② 2NO ( g )+ O 2 ( g ) ![]() 2NO 2 ( g ) ΔH =- 113 . 0 kJ · mol – 1
2NO 2 ( g ) ΔH =- 113 . 0 kJ · mol – 1
则根据盖斯定律可知 (①-②)÷ 2 即得到 NO 2 与 SO 2 反应生成 SO 3 和 NO 的热化学方程式为 NO 2 ( g )+ SO 2 ( g )= SO 3 ( g )+ NO ( g ) △ H =- 41 . 8kJ / mol 。