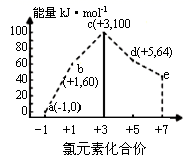
一定条件下,在水溶液中 1 mol Cl - 、 ClO x - (x=1,2,3,4) 的能量 (kJ) 相对大小如图所示。下列有关说法正确的是
A . a、b、c、d、e 中, c 最稳定
B . b→a+c 反应的活化能为反应物能量减生成物能量
C . b→a+d 反应的热化学方程式为: 3ClO(aq)=ClO 3 - (aq)+2Cl - (aq);ΔH=+116 kJ·mol - 1
D . 一定温度下, Cl 2 与 NaOH 溶液反应生成的产物有 a、b、d ,溶液中 a、b、d 的浓度之比可能为 11 ∶ 1 ∶ 2
答案
D
【解析】
根据氯元素的化合价, a、b、c、d、e 依次代表 Cl - 、 ClO - 、 ClO 2 - 、 ClO 3 - 、 ClO 4 - 。 A 项,物质能量越低越稳定,由图可得 a、b、c、d、e 中, a 最稳定 , c 最不稳定,故 A 错误; B 项,反应物能量 - 生成物能量 =-Δ H , 依据图中数据无法判断 b→a+c 反应的活化能,故 B 错误; C 项, a 为 Cl - 、 b 为 ClO - 、 d 为 ClO 3 - , B→A+D 的化学方程式为 3ClO - =ClO 3 - +2Cl - , 结合曲线提供的数据,反应热为 : Δ H =64kJ•mol -1 +2×0kJ•mol -1 -3×60kJ•mol -1 =-116kJ•mol -1 ,故 C 错误 ; D 项,氧化还原反应遵循电子守恒 , Cl 2 与 NaOH 溶液反应生成的产物有 a(Cl - )、b(ClO - )、d(ClO 3 - ), 氯元素化合价由 0 价将为 -1 价、升为 +1 价和 +5 价,由电子守恒得: n(Cl - )=n(ClO - )+5n(ClO 3 - ) ,当溶液中 a、b、d 的浓度之比为 11:1:2 时上述电子守恒式成立,故 D 正确 。
点睛:本题以卤族元素为载体考查了化学反应与能量变化、热化学反应方程式的书写、氧化还原反应等知识 , 关键是弄清 a、b、c、d、e 所代表的离子并正确书写反应的离子方程式,并结合 ΔH= 生成物的总能量 - 反应物的总能量进行计算 , D 项注意氧化还原反应中得失电子守恒 ( 化合价升降总数相等 ) 的应用。


