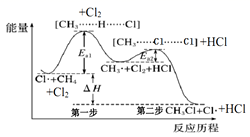
如图 (E a 表示活化能 ) 是 CH 4 与 Cl 2 生成 CH 3 Cl 的部分反应过程中各物质物质的能量变化关系图,下列说法正确的是( )
A . Cl· 可由 Cl 2 在高温条件下生成,是 CH 4 与 Cl 2 反应的催化剂
B . 升高温度, E a1 、 E a2 均减小,反应速率加快
C . 增大 Cl 2 的浓度,可提高反应速率,但不影响 △ H 的大小
D . 第一步反应的速率大于第二步反应
答案
C
【分析】
CH 4 与 Cl 2 生成 CH 3 Cl 的反应方程式为: CH 4 + Cl 2 CH 3 Cl+HCl 。
【详解】
A . Cl· 由 Cl 2 在光照条件下生成,是 CH 4 与 Cl 2 反应的 “中间体”,而不是反应的催化剂, A 错误;
B . E a1 、 E a2 分别为第一步反应、第二步反应所需活化能,升高温度,反应所需活化能不变,即 E a1 、 E a2 不变, B 错误;
C . Cl 2 是该反应的反应物,增大反应物的浓度,反应速率增大,而反应的 △ H 和反应的途径无关,只与反应的始态和终态有关,即增大氯气的浓度不影响 △ H 的大小, C 正确;
D .第一步反应所需活化能 E a1 大于第二步反应所需活化能 E a2 ,第一步反应单位体积内活化分子百分数低于第二步反应,故第二步反应速率更大, D 错误。
答案选 C 。
【点睛】
反应热 △ H 和反应途径无关,只与反应的始态和终态有关。