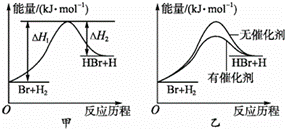
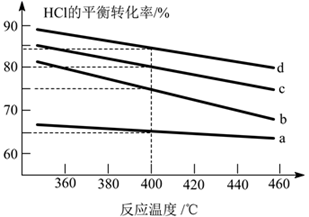
下列有关说法正确的是
A . 已知 HI(g) ![]() 1/2H 2 (g) + 1/2I 2 (s) Δ H =- 26.5 kJ·mol - 1 ,由此可知 1 mol HI 气体在密闭容器中充分分解后可以放出 26.5 kJ 的热量
1/2H 2 (g) + 1/2I 2 (s) Δ H =- 26.5 kJ·mol - 1 ,由此可知 1 mol HI 气体在密闭容器中充分分解后可以放出 26.5 kJ 的热量
B . 已知 2H 2 (g) + O 2 (g)===2H 2 O(g) Δ H =- 571.6 kJ·mol - 1 ,则氢气的燃烧热为 Δ H =- 285.8 kJ·mol - 1
C . 已知 2C(s) + 2O 2 (g)=2CO 2 (g) Δ H 1 , 2C(s) + O 2 (g)=2CO(g) Δ H 2 ,则 Δ H 1 < Δ H 2
D . 含 20.0 g NaOH 的稀溶液与稀盐酸完全中和,放出 28.7 kJ 的热量,则稀醋酸和稀 NaOH 溶液反应的热化学方程式为: NaOH(aq) + CH 3 COOH(aq)===CH 3 COONa(aq) + H 2 O(l) Δ H =- 57.4 kJ·mol - 1
答案
C
【详解】
A. HI(g) ![]() 1/2H 2 (g)+1/2I 2 (s) Δ H =- 26.5 kJ·mol - 1 ,由于反应可逆,可知 1 mol HI气体充分分解后可以放出小于26.5 kJ的热量,故A错误;
1/2H 2 (g)+1/2I 2 (s) Δ H =- 26.5 kJ·mol - 1 ,由于反应可逆,可知 1 mol HI气体充分分解后可以放出小于26.5 kJ的热量,故A错误;
B.根据燃烧热定义可知,水的状态不对,必须为液态才可以,故B错误;
C.已知2C(s)+2O 2 (g)=2CO 2 (g) Δ H 1 , 2C(s)+O 2 (g)=2CO(g) Δ H 2 ,盖斯定律可得: 2CO(g)+O 2 (g)= 2CO 2 (g) Δ H 1 -Δ H 2 ,因为燃烧放热,所以Δ H 1 -Δ H 2 < 0, 则Δ H 1 < Δ H 2 ,故 C正确;
D.因为醋酸为弱电解质,电离需要吸热,所以NaOH(aq)+CH 3 COOH(aq)==CH 3 COONa(aq)+H 2 O(l) ΔH>-57.4 kJ·mol-1,故D错误;
正确答案 :C。
【点睛】
①关于可逆反应热化学方程式注意点:
A.当反应逆向进行,其反应热与正反应的反应热数值相等,符号相反。
B.2SO 2 (g)+O 2 (g) ![]() 2SO 3 (g) ΔH =- a kJ·mol - 1 ,意义是指 2 mol SO 2 气体与 1 mol O 2 完全反应时,放出 a kJ的热量,若将2 mol SO 2 与气体 1 mol O 2 放于一密闭容器中在一定条件下反应达平衡时,放出的热量要小于 a kJ,且当平衡移动(各物质状态不变)时, ΔH 不变。
2SO 3 (g) ΔH =- a kJ·mol - 1 ,意义是指 2 mol SO 2 气体与 1 mol O 2 完全反应时,放出 a kJ的热量,若将2 mol SO 2 与气体 1 mol O 2 放于一密闭容器中在一定条件下反应达平衡时,放出的热量要小于 a kJ,且当平衡移动(各物质状态不变)时, ΔH 不变。
②燃烧热定义:101KPa时,1 mol纯物质完全燃烧生成生成稳定氧化物时所放出的热量;例如氢元素对应液态水,硫元素对应二氧化硫等
中和热定义:稀溶液中强酸跟强碱发生中和反应只生成 1 mol H 2 O时所释放的热量;不同反应物的中和热大致相同,均约为57.3kJ·mol - 1