电解质溶液中存在多种平衡.请回答下列问题:
(1)已知:
| 化学式 |
| HClO |
| 电离常数(25℃) |
|
|
物质的量浓度均为0.1mol/L的下列溶液:a.![]() b.HClO,比较二者
b.HClO,比较二者![]() 的大小:a______b(填“>”、“<”或“=”).
的大小:a______b(填“>”、“<”或“=”).
(2)常温下,将0.1mol/L的![]() 溶液加水稀释,在稀释过程中,下列表达式的数值变大的_________(填字母).
溶液加水稀释,在稀释过程中,下列表达式的数值变大的_________(填字母).
A.![]() B.
B. C.
C.![]()
(3)25℃时,体积均为10mL,pH均为2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程中pH的变化如图所示.
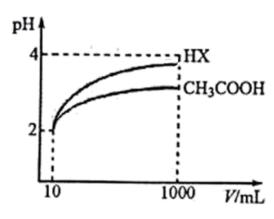
①25℃时,醋酸的电离常数_________HX的电离常数.(填“>”、“<”或“=”)
②稀释100倍后,醋酸溶液中由水电离出的![]() _________HX溶液中由水电离出的
_________HX溶液中由水电离出的![]() .(填“>”、“<”或“=”)
.(填“>”、“<”或“=”)
(4)已知:二元酸![]() 的电离方程式是:
的电离方程式是:![]() ,若
,若![]() 溶液的
溶液的![]() ,则
,则![]() 溶液中
溶液中![]() 是__________
是__________
A.小于![]() B.大于
B.大于![]() C.等于
C.等于![]() D.等于
D.等于![]()
答案
> B < < A
【详解】
(1)相同浓度的CH3COOH和HClO,CH3COOH的电离常数大,反应的完全程度更高,电离出的H+浓度更大,所以a>b;
(2)A.稀释促进电离,对于电离平衡CH3COOH![]() CH3COO-+H+,加水稀释后,平衡正向移动,n(CH3COO-)、n(H+)增大,n(CH3COOH)减小,但是因为加水稀释,体积的增大成为主导因素,所以cCH3COO-)、c(H+)、c(CH3COOH)均减小,A项错误;
CH3COO-+H+,加水稀释后,平衡正向移动,n(CH3COO-)、n(H+)增大,n(CH3COOH)减小,但是因为加水稀释,体积的增大成为主导因素,所以cCH3COO-)、c(H+)、c(CH3COOH)均减小,A项错误;
B.根据![]() ,得
,得 ,温度不变,Ka不变,c(H+)减小,所以
,温度不变,Ka不变,c(H+)减小,所以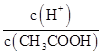 增大,B项正确,
增大,B项正确,
C.温度不变,Kw不变,所以![]() 不变,C项错误;
不变,C项错误;
选择B;
(3)①由图像知,pH相同的醋酸和HX均从10mL稀释到了1000mL,稀释了100倍,HX的pH值变化更大,所以HX的电离程度更高,酸性更强,电离常数更大;
②稀释100倍后,HX的pH更大,溶液中c(H+)更小,此时H+主要有溶质HX的电离提供,根据Kw=![]() ,知HX溶液中的c(OH-)更大,此时的OH-完全来源于水的电离,所以,由水电离出的c(H+)与溶液中的c(OH-)相同,所以HX溶液中由水电离出的c(H+)更大,答案为<;
,知HX溶液中的c(OH-)更大,此时的OH-完全来源于水的电离,所以,由水电离出的c(H+)与溶液中的c(OH-)相同,所以HX溶液中由水电离出的c(H+)更大,答案为<;
(4) NaHR在水溶液中的电离方程式为:![]() ,溶液中的H+主要来源于HR-的电离,可以认为HR-电离出的
,溶液中的H+主要来源于HR-的电离,可以认为HR-电离出的![]() ,又
,又![]() 中的H+来源于两部分,H2R的电离和HR-的电离,所以
中的H+来源于两部分,H2R的电离和HR-的电离,所以![]() 可以电离出0.1mol/LH+和0.1mol/L HR-,0.1mol/L HR-则可以电离出amol/L的H+,因为第一步电离出的H+对第二步电离有抑制作用,所以0.1mol/L HR-电离出的H+浓度小于amol/L,所以
可以电离出0.1mol/LH+和0.1mol/L HR-,0.1mol/L HR-则可以电离出amol/L的H+,因为第一步电离出的H+对第二步电离有抑制作用,所以0.1mol/L HR-电离出的H+浓度小于amol/L,所以![]() 电离出的H+总浓度小于(0.1+a)mol/L,选择A
电离出的H+总浓度小于(0.1+a)mol/L,选择A
【点睛】
水溶液中的平衡,应当抓住主要因素来分析,比如弱酸的电离平衡,稀释主要引起了溶液体积的变化;稀释促进电离,稀释促进水解。

