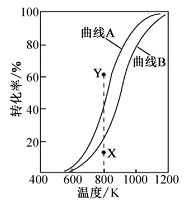
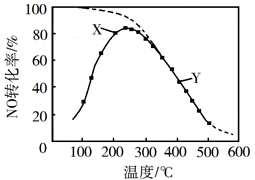
在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
A.反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
答案
BD
【详解】
A.随温度升高NO的转化率先升高后降低,说明温度较低时反应较慢,一段时间内并未达到平衡,分析温度较高时,已达到平衡时的NO转化率可知,温度越高NO转化率越低,说明温度升高平衡向逆方向移动,根据勒夏特列原理分析该反应为放热反应,∆H<0,故A错误;
B.根据上述分析,X点时,反应还未到达平衡状态,反应正向进行,所以延长反应时间能提高NO的转化率,故B正确;
C.Y点,反应已经达到平衡状态,此时增加O2的浓度,使得正反应速率大于逆反应速率,平衡向正反应方向移动,可以提高NO的转化率,故C错误;
D.设NO起始浓度为amol/L,NO的转化率为50%,则平衡时NO、O2和NO2的浓度分别为0.5amol/L、(5×10-4-0.25a)mol/L、0.5amol/L,根据平衡常数表达式K=![]() >
>![]() =2000,故D正确;
=2000,故D正确;
故选BD。
【点睛】
解本题时需要注意:实线中在最高点之前反应没有达到平衡状态,主要讨论温度对化学反应速率的影响;最高点之后反应达到平衡状态,可以研究温度对化学平衡的影响。

 pC(g)+qD(g)
pC(g)+qD(g)  。
。 时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。
时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。 指的是同一物质的正反应速率与逆反应速率相等。
指的是同一物质的正反应速率与逆反应速率相等。  qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。
qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。