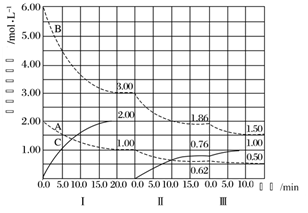
根据vt图分析外界条件改变对可逆反应A(g)+3B(g) ![]() 2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
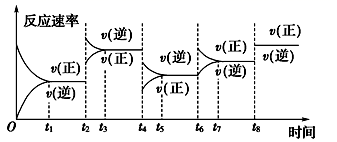
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是
A.使用了催化剂、增大压强、减小反应物浓度、降低温度
B.升高温度、减小压强、减小反应物浓度、使用了催化剂
C.增大反应物浓度、使用了催化剂、减小压强、升高温度
D.升高温度、减小压强、增大反应物浓度、使用了催化剂
答案
D
【分析】
从“断点”入手突破改变的条件,t2时正、逆反应速率均增大,且平衡逆向移动,不是使用了催化剂,排除A,增大反应物浓度,平衡正向移动,排除C,t6时正反应速率大于逆反应速率,逆反应速率瞬时不变,应是增大反应物浓度,排除B。
【详解】
t2时正、逆反应速率均增大,且平衡逆向移动,排除A、C项;t4时正、逆反应速率均减小,平衡逆向移动,可以是减小压强;t6时正反应速率大于逆反应速率,逆反应速率瞬时不变,平衡正向移动,所以是增大反应物浓度,D项符合。故选D。

 pC(g)+qD(g)
pC(g)+qD(g)  。
。 时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。
时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。 指的是同一物质的正反应速率与逆反应速率相等。
指的是同一物质的正反应速率与逆反应速率相等。  qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。
qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。