利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)![]() CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示,下列说法正确的是( )
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示,下列说法正确的是( )
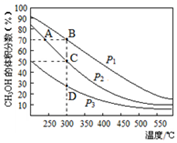
A.该反应的△H<0,且p1<p2<p3
B.在C点时,H2转化率为75%
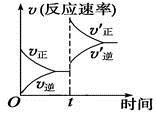
C.反应速率:ν逆(状态A)>ν逆(状态B)
D.在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,达平衡时CH3OH的体积分数增大
答案
B
【解析】
试题分析:A.升高温度,CH3OH的体积分数减小,平衡逆向移动,说明正反应为放热反应,△H<0,该反应为气体体积减小的反应,增大压强,平衡正向移动,可以提高CH3OH的体积分数,则p2<p1,A项错误;
B.设起始时CO的物质的量为1mol,则H2的物质的量为2mol。在C点,假设反应的CO的物质的量为x

平衡时总的物质的量为:(1-x)+(2-2x)+x=3-2x。甲醇的体积分数为50%,则![]() ×100%=50%,解得x=0.75,因此CO转化率为75%,B项正确;
×100%=50%,解得x=0.75,因此CO转化率为75%,B项正确;
C.温度越高,反应速率越快,B的反应温度高,反应速率:ν逆(状态A)<ν逆(状态B),C项错误;
D.在恒温恒压条件下向密闭容器中充入不同量的CH3OH,根据等效平衡的建立条件,达平衡时CH3OH的体积分数相同,D项错误;
答案选B。