在容积可变的密闭容器中充入2mol A和1mol B发生反应:mA(g) + nB(g) ![]() pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
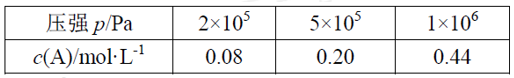
A.维持压强2×105Pa,若反应开始后5min时达到平衡,则v(A)=0.016mol/(L·min)
B.P从2×105Pa增加到5×105Pa时,平衡逆向移动
C.P为1×106Pa时,平衡常数表达式K=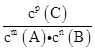
D.其它条件相同时,在上述三个压强下分别发生该反应。A的转化率随时间变化曲线如图所示

答案
D
【分析】
由气体状态方程PV=nRT,得P=![]() RT即P=cRT,当温度相同时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,所以气体物质的计量数关系应为m+n=p。压强从5×105Pa增大到1×106Pa时,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol>0.4mol,浓度增大超过了2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面的分析,说明B在高压下变成液态或固体,由此分析解答。
RT即P=cRT,当温度相同时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,所以气体物质的计量数关系应为m+n=p。压强从5×105Pa增大到1×106Pa时,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol>0.4mol,浓度增大超过了2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面的分析,说明B在高压下变成液态或固体,由此分析解答。
【详解】
A.题目中没有给出初始时容器体积,无法计算反应物A的初始浓度,也就无法计算在此条件下用A表示的反应速率,A项错误;
B.由气体状态方程PV=nRT,得P=![]() RT即P=cRT,当温度一定时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,B项错误;
RT即P=cRT,当温度一定时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,B项错误;
C.由B项分析可知压强从2×105Pa增大到5×105Pa时平衡没有移动,说明反应前后气体分子数相等,即m+n=p;再从表格数据看,压强从5×105Pa增大到1×106Pa,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol,浓度增大的倍数大于2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面分析可推断B在此压强下变成了液体或固体,所以压强为1×106Pa时B不是气体,其浓度视为常数,在平衡常数表达式中不应出现,即K=![]() ,C项错误;
,C项错误;
D.其它条件相同时,对于气体参加的反应增大压强反应速率增大,所以压强分别为1×106Pa、5×105Pa、2×105Pa下达到平衡(拐点)时所用时间依次增大;由B项分析知压强从2×105Pa增大到5×105Pa平衡没有移动,A的转化率相同;由C项分析知压强从5×105Pa增大到1×106Pa平衡向逆反应方向移动,A的转化率减小,图像与事实相符,D项正确;
答案选D。
【点睛】
我们在记忆阿伏加德罗定律及其推论时可以从理想气体状态方程角度理解和分析,因为描述气体有四个物理量就够了:P、T、V、n,它们之间关系就是状态方程PV=nRT(R普适气体常数),如当温度和体积相同时,气体的压强与气体物质的量(即粒子数)成正比等。

 2SO3中通入He,平衡逆向移动原因:体积增大,压强不变,浓度减小,平衡逆向移动。
2SO3中通入He,平衡逆向移动原因:体积增大,压强不变,浓度减小,平衡逆向移动。  随时间(含条件改变对化学反应速率的影响)变化的观律,体现了平衡的“动、等、定、变”的基本特征,以及平衡移动的方向等。
随时间(含条件改变对化学反应速率的影响)变化的观律,体现了平衡的“动、等、定、变”的基本特征,以及平衡移动的方向等。




 bB(g)+ cc(g),增加A的量,平衡向正反应方向移动,但反应物 A的转化率与气体物质的化学计量数有关:
bB(g)+ cc(g),增加A的量,平衡向正反应方向移动,但反应物 A的转化率与气体物质的化学计量数有关:
 cC(g)+dD(g):
cC(g)+dD(g): 

 ,压强的变化对其平衡无影响。这是因为,在这种情况下,压强的变化对正、逆反应速率的影响程度是等同的,故平衡不移动。
,压强的变化对其平衡无影响。这是因为,在这种情况下,压强的变化对正、逆反应速率的影响程度是等同的,故平衡不移动。  ,
, ,当浓度同时增大一倍时,即让
,当浓度同时增大一倍时,即让
 ,此时相当于压强增大一倍,平衡向生成NH3的方向移动。
,此时相当于压强增大一倍,平衡向生成NH3的方向移动。 
 ,平衡后,向容器中再通入反应物
,平衡后,向容器中再通入反应物 ,使 c(NO2)增大,平衡正向移动;如向容器中再通入生成物 N2O4,则使c(N2O4)增大,平衡逆向移动。但由于两种情况下,容器内的压强都增大,故对最终平衡状态的影响是一致的,如两种情况下,重新达到平衡后,NO2的百分含量都比原平衡时要小
,使 c(NO2)增大,平衡正向移动;如向容器中再通入生成物 N2O4,则使c(N2O4)增大,平衡逆向移动。但由于两种情况下,容器内的压强都增大,故对最终平衡状态的影响是一致的,如两种情况下,重新达到平衡后,NO2的百分含量都比原平衡时要小