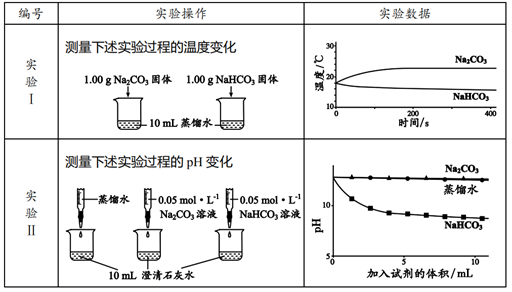
碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称________,可作为碱使用的原因是___________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)= Na2CO3(s)+H2O(g) ΔH1=−127.4 kJ·mol−1
②NaOH(s)+CO2(g)= NaHCO3(s) ΔH1=−131.5 kJ·mol−1
反应2NaHCO3(s)= Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=_______ kJ·mol−1,该反应的平衡常数表达式K=________。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中![]() =_____________。已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10。
=_____________。已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10。
答案
纯碱或苏打 CO32-+H2O![]() HCO3-+OH- 135.6 c(H2O)×c(CO) 24
HCO3-+OH- 135.6 c(H2O)×c(CO) 24
【解析】
(1)碳酸钠俗称纯碱和苏打,碳酸钠属于强碱弱酸盐,CO32-发生水解反应,其水解方程式为:CO32-+H2O![]() HCO3-+OH-,溶液显碱性;(2)①-2×②得到:2NaHCO3(s)=Na2CO3(s)+CO2(g)+H2O(g) △H=(-127.4+2×131.5)kJ·mol-1=+135.6kJ·mol-1,Na2CO3和NaHCO3为固体,根据化学平衡常数的定义K= c(H2O)×c(CO);(4)在同一个溶液中,c(Ba2+)相同,依据溶度积的数学表达式,则有
HCO3-+OH-,溶液显碱性;(2)①-2×②得到:2NaHCO3(s)=Na2CO3(s)+CO2(g)+H2O(g) △H=(-127.4+2×131.5)kJ·mol-1=+135.6kJ·mol-1,Na2CO3和NaHCO3为固体,根据化学平衡常数的定义K= c(H2O)×c(CO);(4)在同一个溶液中,c(Ba2+)相同,依据溶度积的数学表达式,则有![]() =24。
=24。