研究表明,在催化剂a(或催化剂b)存在下,CO2和H2能同时发生两个平行反应,反应的热化学方程式如下:
① CO2(g)+ 3H2(g)![]() CH3OH(g)+ H2O(g) ΔH1= − 53.7 kJ/mol
CH3OH(g)+ H2O(g) ΔH1= − 53.7 kJ/mol
② CO2(g)+ H2(g)![]() CO(g)+ H2O(g) ΔH2= + 41.2 kJ/mol
CO(g)+ H2O(g) ΔH2= + 41.2 kJ/mol
某实验小组控制CO2和H2初始投料比为1∶2.2。在相同压强下,经过相同反应时间测得的实验数据如下:
| 实验编号 | T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 1 | 543 | 催化剂a | 12.3 | 42.3 |
| 2 | 543 | 催化剂b | 10.9 | 72.7 |
| 3 | 553 | 催化剂a | 15.3 | 39.1 |
| 4 | 553 | 催化剂b | 12.0 | 71.6 |
(备注)甲醇选择性:转化的CO2中生成甲醇的百分比。下列说法不正确的是
A.相同温度下,在该时刻催化剂b对CO2转化成CH3OH有较高的选择性
B.其他条件不变,升高温度反应①中CO2转化为CH3OH平衡转化率增大
C.其他条件不变,增大反应体系压强反应②中平衡常数不变
D.反应①在无催化剂、有催化剂a和有 催化剂b三种情况下能量示意图如下: 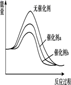
答案
B
【详解】
A.根据实验1和2、实验3和4的实验数据进行对比,相同温度下,催化剂b对CO2转化成CH3OH的数据较高,则催化剂b对CO2转化成CH3OH有较高的选择性,故A正确;
B.反应①为放热反应,其他条件不变,升高温度,反应①向逆向移动,CO2转化为CH3OH平衡转化率减小,故B错误;
C.平衡常数与温度相关,温度不变,平衡常数不变。则其他条件不变,增大反应体系压强,反应②中平衡常数不变,,故C正确;
D.从表中的数据分析,在催化剂b的作用下,甲醇的选择性更大,说明催化剂b对反应①催化效果更好,催化剂能降低反应的活化能,说明使用催化剂b的反应过程中活化能更低,故D正确。答案选B。
