水的电离平衡曲线如右图所示,下列说法中,正确的是

A. 图中A、B、D三点处KW间的关系: B>A>D
B. 100℃,向pH=2的稀硫酸中逐滴加入等体积pH=10的稀氨水,溶液中 c(NH4+)/c(NH3·H2O)减小,充分反应后,溶液到达B点
C. 温度不变,在水中加入适量NH4Cl固体,可从A点变化到C点
D. 加热浓缩A点所示溶液,可从A点变化到B点
答案
D
【解析】A. Kw=c(H+)c(OH-),KW仅是温度的函数,且随温度升高而增大,所以图中A、B、D三点处KW间的关系:B>A=D,故A错误;
B.100℃时,Kw=10-12,向pH=2 的稀硫酸中逐滴加入等体积pH=10 的稀氨水后,溶液中c(OH-)增大,而一水合氨的电离平衡常数Kb= 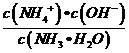 不变,故
不变,故![]() 减小;而最终氨水过量,溶液显碱性,反应后溶液不能达到B点,故B错误;
减小;而最终氨水过量,溶液显碱性,反应后溶液不能达到B点,故B错误;
C.温度不变,在水中加入适量NH4Cl 固体,溶液由中性变为酸性,而C点也显中性,故溶液不能由A变为C点,故C错误;
D.加热浓缩A点溶液,由于A点溶液显中性,故加热浓缩后仍显中性,且升高温度,Kw增大,故可以到达B点,故D正确;
故选D。

 NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。
NH4++NH2-,由于液氨的自偶电离程度比水要弱,所以是非电解质。