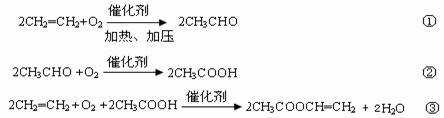
以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵【(NH4)3Fe(C6H5O7)2】。
(1)Fe基态核外电子排布式为___________;![]() 中与Fe2+配位的原子是________(填元素符号)。
中与Fe2+配位的原子是________(填元素符号)。
(2)NH3分子中氮原子的轨道杂化类型是____________;C、N、O元素的第一电离能由大到小的顺序为_______________。
(3)与NH![]() 互为等电子体的一种分子为_______________(填化学式)。
互为等电子体的一种分子为_______________(填化学式)。
(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_________mol。
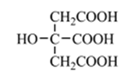
答案
(1). 1s22s22p63s23p63d64s2或[Ar]3d64s2 (2). O (3). sp3 (4). N>O>C (5). CH4或SiH4 (6). 7
【解析】
【分析】
(1)Fe核外有26个电子,H2O中O原子有孤对电子,提供孤对电子。
(2)先计算NH3分子中氮原子价层电子对数,同周期,从左到右,第一电离能呈增大的趋势,但第IIA族大于第IIIA族,第VA族大于第VIA族。
(3)根据价电子数Si=C=N+的关系得出![]() 互为等电子体的分子。
互为等电子体的分子。
(4)羧基的结构是![]() ,一个羧基中有碳原子与氧原子分别形成两个σ键,一个羟基与碳原子相连形成一个σ键。
,一个羧基中有碳原子与氧原子分别形成两个σ键,一个羟基与碳原子相连形成一个σ键。
【详解】(1)Fe核外有26个电子,其基态核外电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2;由于H2O中O原子有孤对电子,因此[Fe(H2O)6]2+中与Fe2+配位的原子是O;故答案为:1s22s22p63s23p63d64s2或[Ar]3d64s2;O。
(2)NH3分子中氮原子价层电子对数为![]() ,因此氮杂化类型为sp3,同周期,从左到右,第一电离能呈增大的趋势,但第IIA族大于第IIIA族,第VA族大于第VIA族,因此C、N、O元素的第一电离能由大到小的顺序为N>O>C;故答案为:sp3;N>O>C。
,因此氮杂化类型为sp3,同周期,从左到右,第一电离能呈增大的趋势,但第IIA族大于第IIIA族,第VA族大于第VIA族,因此C、N、O元素的第一电离能由大到小的顺序为N>O>C;故答案为:sp3;N>O>C。
(3)根据价电子数Si=C=N+,得出![]() 互为等电子体的分子是CH4或SiH4;故答案为:CH4或SiH4。
互为等电子体的分子是CH4或SiH4;故答案为:CH4或SiH4。
(4)羧基的结构是![]() ,一个羧基中有碳原子与氧原子分别形成两个σ键,三个羧基有6个,还有一个羟基与碳原子相连形成一个σ键,因此1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为7mol;故答案为:7。
,一个羧基中有碳原子与氧原子分别形成两个σ键,三个羧基有6个,还有一个羟基与碳原子相连形成一个σ键,因此1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为7mol;故答案为:7。
【点睛】物质结构是常考题型,主要考查电子排布式,电离能、电负性、共价键分类、杂化类型、空间构型等。