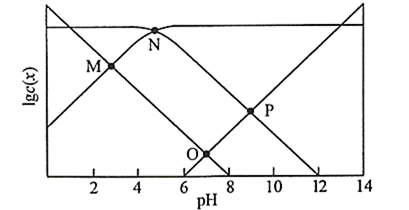
25℃时,某混合溶液中![]() ,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是
,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是
A. O点时,![]()
B. N点时,![]()
C. 该体系中,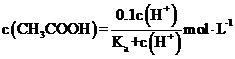
D. pH由7到14的变化过程中, CH3COO-的水解程度始终增大
答案
BC
【解析】
【分析】
根据图像分析可知,随着pH的升高,氢氧根离子和醋酸根离子浓度增大,氢离子和醋酸离子浓度减小,又pH=7的时候,氢氧根离子浓度等于氢离子浓度,故可推知,图中各曲线 代表的浓度分别是:曲线1为lgc(CH3COO-)随pH的变化曲线,曲线2为lgc(H+)随pH的变化曲线,曲线3为lgc(OH-)随pH的变化曲线,曲线4为lgc(CH3COOH)随pH的变化曲线,据此结合水溶液的平衡分析作答。
代表的浓度分别是:曲线1为lgc(CH3COO-)随pH的变化曲线,曲线2为lgc(H+)随pH的变化曲线,曲线3为lgc(OH-)随pH的变化曲线,曲线4为lgc(CH3COOH)随pH的变化曲线,据此结合水溶液的平衡分析作答。
【详解】A. 根据上述分析可知,O点为曲线2和曲线3的交点,对应的pH=7,应该得出的结论为:c(H+)= c(OH-),故A错误;
B. N点为曲线1和曲线4的交点, lgc(CH3COO-)=lgc(CH3COOH),即c(CH3COO-)=c(CH3COOH),因Ka=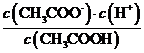 ,代入等量关系并变形可知pH=-lgKa,故B正确;
,代入等量关系并变形可知pH=-lgKa,故B正确;
C. c(CH3COO-)+c(CH3COOH)=0.1mol/L,则c(CH3COO-)=0.1mol/L- c(CH3COOH),又Ka=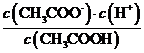 ,联立两式消去c(CH3COO-)并化简整理可得出,c(CH3COOH)=
,联立两式消去c(CH3COO-)并化简整理可得出,c(CH3COOH)=![]() mol/L,故C正确;
mol/L,故C正确;
D. 醋酸根离子的水解平衡为:CH3COO-+H2O![]() CH3COOH +OH-,pH由7到14的变化过程中,碱性不断增强,c(OH-)不断增大,则使不利于醋酸根离子的水解平衡,会使其水解程度减小,故D错误;
CH3COOH +OH-,pH由7到14的变化过程中,碱性不断增强,c(OH-)不断增大,则使不利于醋酸根离子的水解平衡,会使其水解程度减小,故D错误;
答案选BC。