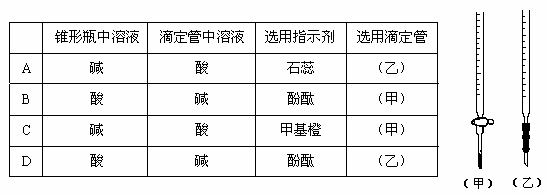
应用酸碱中和滴定原理测定某市售白醋的含量。
I.实验步骤
(I)量取10.00mL食用白醋,稀释到100mL,得到待测白醋溶液,取待测白醋溶液20.00mL于锥形瓶中,向其中滴加几滴________作指示剂。
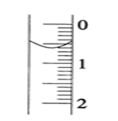
(2)碱式滴定管盛装0.1000mol/LNaOH溶液初始时的液面位置如图所示,此时的读数_____mL。
(3)滴定过程中,滴至_________________时即为滴定终点,记录NaOH溶液的最终读数。重复滴定4次。
Ⅱ.实验记录
| 实验序号 | 待测白醋溶液体积/mL | 0.1000mol/LNaOH溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 20.00 | 0.10 | l5.10 |
| 2 | 20.00 | 0.00 | 14.95 |
| 3 | 20.00 | 0.15 | 15.20 |
| 4 | 20.00 | 1.10 | 17.10 |
Ⅲ.数据处理与讨论
(4)按实验所得数据,可折算得c(市售白醋)=__________mol/L。
(5)在本实验的滴定过程中,下列操作会使实验结果偏大的是________(填选项字母)。
a.碱式滴定管在装液前未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气池,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
答案
(1). 酚酞 (2). 0.60 (3). 溶液由无色恰好变为浅红色,且半分钟内不褪色 (4). 0.07500 (5). ab
【解析】
【分析】
(1)强碱滴定弱酸,达到终点时溶液为强碱弱酸盐,显碱性,结合指示剂变色范围选择合适的指示剂;
(2)根据滴定管的结构和精确度来解答;
(3)滴定过程中眼睛需要观察锥形瓶中溶液颜色变化,判定滴定终点,溶液由无色恰好变为红色,并在半分钟内不褪色;
(4)先根据数据![]() 有效性,然后计算消耗标准液平均体积,依据c(待测)=
有效性,然后计算消耗标准液平均体积,依据c(待测)=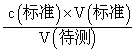 ,计算醋酸浓度;
,计算醋酸浓度;
(5)分析操作对消耗标准液体积的影响,依据c(待测)=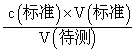 进行误差分析。
进行误差分析。
【详解】(1)用氢氧化钠溶液滴定醋酸溶液,滴定达到终点时生成的醋酸钠溶液,显碱性,酚酞变色范围为8.2-10.0,为减小误差,应选择酚酞做指示剂;
(2)滴定管小数在上部,大数在下部,精确度为0.01mL,所以图中读数为:0.60mL;
(3)滴定过程中需要观察液颜色变化,当溶液由无色恰好变为红色,并在半分钟内不褪色为滴定终点;
(4)四次实验消耗标准液体积分别为:15.00mL;14.95mL;15.05mL;17mL;第四组数据误差较大,应该舍弃,则消耗NaOH标准液体积为V(NaOH)=![]() mL=15.00mL,则根据滴定公式可得待测醋酸溶液的浓度c(CH3COOH)=
mL=15.00mL,则根据滴定公式可得待测醋酸溶液的浓度c(CH3COOH)=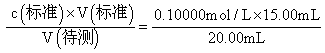 =0.07500mol/L;
=0.07500mol/L;
(5)a.碱式滴定管在装液前未用标准NaOH溶液润洗,导致消耗标准液体积偏大,依据c(待测)=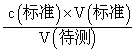 可知,溶液浓度偏大,a符合题意;
可知,溶液浓度偏大,a符合题意;
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失,导致消耗标准液体积偏大,依据c(待测)=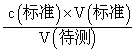 可知,溶液浓度偏大,b符合题意;
可知,溶液浓度偏大,b符合题意;
c.锥形瓶中加入待测白醋溶液后,再加少量水,对消耗标准液体积不产生影响,依据c(待测)=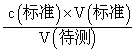 可知,对待测溶液浓度无影响,c不符合题意;
可知,对待测溶液浓度无影响,c不符合题意;
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出,导致消耗标准液体积偏小,依据c(待测)=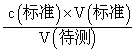 可知,导致待测溶液浓度偏小,d不符合题意;
可知,导致待测溶液浓度偏小,d不符合题意;
故合理选项是ab。
【点睛】本题主要考查了中和滴定的有关知识。涉及指示剂的选择、仪器的选择、误差分析等,注意把握中和滴定实验的原理,根据反应产生的溶液的酸碱性选择合适的指示剂,注意根据物质的量浓度公式进行误差分析,把实验操作的影响都归结在对消耗标准NaOH溶液的体积上分析,若V(NaOH)偏大,则会导致待测溶液的浓度偏高,反之则偏低。




 可知,
可知, 是准 确量取的体积,
是准 确量取的体积, 是标准溶液的浓度,它们均为定值,所以
是标准溶液的浓度,它们均为定值,所以 的大小取决于
的大小取决于 的大小,
的大小, 大则
大则 大,
大, 小则
小则 小。
小。